28.(15分) 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:
CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g)  CH3OH(g) +
H2O(g) ΔH2
CH3OH(g) +
H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为
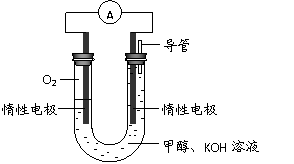 (3)某实验小组依据甲醇燃烧的反应原理,
(3)某实验小组依据甲醇燃烧的反应原理,
设计如右图所示的电池装置。
① 该电池正极的电极反应为
。
② 工作一段时间后,测得溶液的
pH减小,该电池总反应的化学方程式为
。
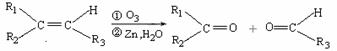 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)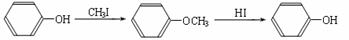
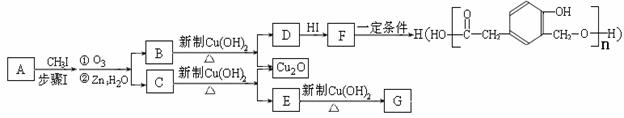 某种芳香族化合物A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去。
某种芳香族化合物A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去。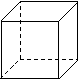 ⑵金属Pt内部原子的堆积方式与铜及干冰中CO2相同,右图正方体是Pt晶胞示意图,叙述Pt原子在晶胞中位置:
⑵金属Pt内部原子的堆积方式与铜及干冰中CO2相同,右图正方体是Pt晶胞示意图,叙述Pt原子在晶胞中位置: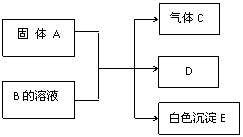 A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示: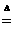 2CaSO4+2Cl2↑+2H2O
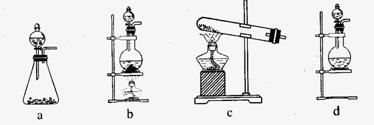
。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O
。他们设计了如下制取氯气并验证其性质的实验。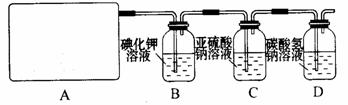
 C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol。以下叙述中不正确的是(
)
C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol。以下叙述中不正确的是(
)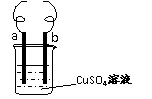 用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如右图所示。则下列说法正确的是
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如右图所示。则下列说法正确的是