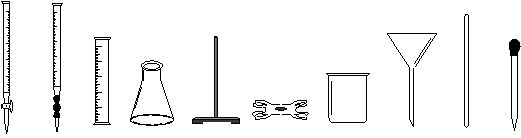
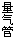(四)请你参与以下探究
(1)实验A反应速度明显比B小,原因是
(2)根据“铜位于金属活动顺序表氢之后,与稀盐酸不反应,而在实验C中加热时又产生气体”的事实,作出如下推断:
①有同学认为“实验C中加热时产生的气体是溶解在溶液中的H2”,你认为是否有道理,理由是 。
②某同学作了如下猜想:是否成立?请你设计实验方案加以验证。
|
猜想 |
验证方法 |
预测现象及结论 |
|
认为铜片中可能含有锌等杂质 |
|
|
(3)某同学对实验D中的白色沉淀进行分析:“不可能是CuCl2,因为CuCl2能溶于水且溶液显蓝色;也不可能是ZnCl2,因为稀释后溶液更稀,不会析出ZnCl2晶体。若利用资料卡片资料①②大胆猜想,白色沉淀可能是CuCl。请你帮他设计验证方案(若有多处方案,只设计两个)。
|
猜想 |
预设验证方法 |
猜想的现象与结论 |
|
白色沉淀 是氯化亚铜 |
|
|
|
|
|
(4)指导老师肯定了实验D中的白色沉淀是CuCl;并指出生成沉淀的原因,实际上是[CuCl4]3-等离子与CuCl(s)、Cl-三者之间所形成的沉淀溶解平衡移动的结果。请写出这一平衡关系式(用离子方程式表示)
。
26、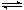 (10分)已知NO2和N2O4可以相互转化:2NO2(g)
N2O4(g); △H<0。现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。
(10分)已知NO2和N2O4可以相互转化:2NO2(g)
N2O4(g); △H<0。现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。
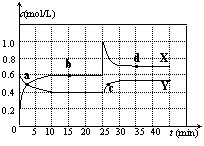 (1)图中共有两条曲线X和Y,其中曲线 表示NO2
(1)图中共有两条曲线X和Y,其中曲线 表示NO2
浓度随时间的变化;a、b、c、d四个点中,表示化学反应处
于平衡状态的点是 。
(2)①前10min内用NO2表示的化学反应速率
v(NO2)= mol/(L·min)
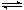 ②15min时,反应2NO2(g) N2O4(g)在b点的浓度
②15min时,反应2NO2(g) N2O4(g)在b点的浓度
平衡常数K(b)=
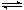 ③35min时,反应2NO2(g) N2O4(g)在d点的浓度平衡常数K(d) K(b)
③35min时,反应2NO2(g) N2O4(g)在d点的浓度平衡常数K(d) K(b)
(填“>”、“=”或“<”)
(3)①若要达到使NO2(s)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是 。
A、加入催化剂 B、缩小容器体积 C、升高温度 D、加入一定量的N2O4
②若在35min时,保持温度不变,快速缩小玻璃容器的体积至1L,气体的颜色变化过程是 。
(三)背景资料
|
资料卡片 主题:生成一价铜的反应 ① 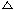 必修一,P116:4CuO
=== 2Cu2O + O2↑ 必修一,P116:4CuO
=== 2Cu2O + O2↑② 《无机化学》下册,p705:2Cu2+ + 4I- == 2CuI(白色)↓+ I2 ③ 《无机化学》下册,p706:氯化亚铜(CuCl)在不同浓度的KCl溶液中可形成[CuCl4]3+等无色离子。 |
(二) 实验记录:
|
交流卡片 主题:Zn、Cu与浓盐酸间的实验 A.将锌放入浓盐酸间的实验 B. 将锌与铜片贴在一起,一同放入浓盐酸中,反应快速放出气体 C. 当实验B中锌片完全溶解后,将溶液加热,又产生大量气体,得到无色溶液 D.将实验C反应后的溶液隔绝空气,加入适量水,出现白色沉淀 |
23、(8分)氯磺酸(ClSO3H)和甲酸(HCOOH)的有关性质如下表:
|
|
颜色、状态 |
沸点(℃) |
密度(g/cm3) |
特性 |
|
氯磺酸 |
无色或淡黄色油状液体 |
151 |
1.77 |
在空气中“发烟”,遇水起剧烈作用 |
|
甲酸 |
无色液体 |
100.8 |
1.22 |
在空气中“发烟”,有强腐蚀性 |
它们可发生反应:HCOOH + ClSO3H == CO↑+ HCl↑+ H2SO4。请用具支试管(

 试管侧壁有一支管)、单孔橡皮塞、玻璃导管、尖嘴玻璃导管及橡胶管来设计一套实验装置,实验目的要求:
试管侧壁有一支管)、单孔橡皮塞、玻璃导管、尖嘴玻璃导管及橡胶管来设计一套实验装置,实验目的要求:
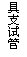
 ①混合氯磺酸和甲酸制取CO;
①混合氯磺酸和甲酸制取CO;
②用制得的CO还原氧化铜;
③无污染。
(1)实验装置的一部分已画于图
中的方框内,试将该实验装置补充
完整并注明所装的药品(不必画夹
持装置)。
(2)实验中混合甲酸和氯磺酸的具体操作方法是
;混合液体分上、下两层,在两层液体的界面处有少量气泡;轻轻振荡试管,可以加快气泡产生的速率。加快反应速率的可能原因是
。
22、(10分)某同学设计下图装置进行探究。(夹持装置已略去)
(1)进行“铜和稀硝酸反应制取NO”的实验。
①制取NO的化学方程式:
②收集气体前必须先 然后才开始收
集气体。
(2)利用该装置制取并收集少量其他气体,请完成下表:
|
制取气体 |
药品 |
|
O2 |
、
|
|
|
某溶液、Al |
(3)利用该装置进行实验,并根据产生氢气的量来确定某酸的结构:
①反应前,先对量气管进行第一次读数。读数时,应注意的操作是
,并使视线与凹液面最低处相平;反应后,待 时,再对量气管进行第二次读数。
②实验数据记录如下:(表中读数已折合成标准状况下的数值)
|
编号 |
酸的质量 |
金属锌的质量 |
量气管第一次读数 |
量气管第二次读数 |
|
1 |
1.45g |
10.0g(足量) |
40mL |
264mL |
|
2 |
1.45g |
10.0g(足量) |
30mL |
228mL |
|
3 |
1.44g |
10.0g(足量) |
20mL |
243mL |
已知该酸的相对分子质量为145。根据上述数据可确定该酸是 元酸;
③如果第二次对量气管读数时仰视,则测得的气体体积会 (填“偏高”、“偏低”或“不能确定”)
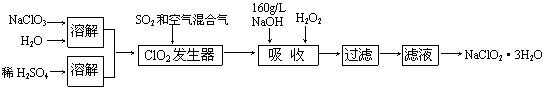 (9分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
(9分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图: