17.(6分)室温下,向一定量的稀氨水中逐滴加入物质的量浓度相同的盐酸,直至盐酸过
量。
(1)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”)
(2)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH。试填写表中空白:
|
|
离子浓度由大到小的顺序 |
溶质的化学式 |
溶液的pH |
|
① |
c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
|
pH>7 |
|
② |
c(NH4+)=c(Cl-) |
NH4Cl、NH3·H2O |
|
|
③ |
|
NH4Cl |
pH<7 |
|
④ |
c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
|
pH<7 |
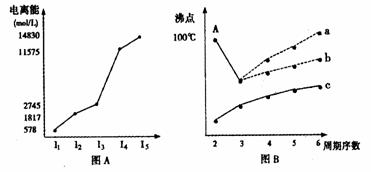 族。
族。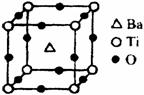 II.在Ti的化合物中,可以呈现+2、+3、+4三种化合价,
II.在Ti的化合物中,可以呈现+2、+3、+4三种化合价,
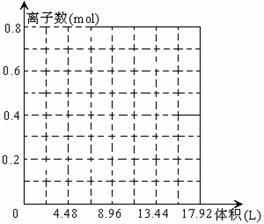 (3)某溶液中有和0.2mol KOH 0.1mol Ca(OH)2, 往溶液中持续通入CO2, 当CO2刚足量时,立即改通NH3, 作出通入气体总体积与溶液中离子总数的图象。(不考虑气体在水中的溶解度,离子水解和水的电离均忽略不计)
(3)某溶液中有和0.2mol KOH 0.1mol Ca(OH)2, 往溶液中持续通入CO2, 当CO2刚足量时,立即改通NH3, 作出通入气体总体积与溶液中离子总数的图象。(不考虑气体在水中的溶解度,离子水解和水的电离均忽略不计) (1)硫酸生产中,SO2催化氧化生成SO3: 2SO2(g)+O2(g)
(1)硫酸生产中,SO2催化氧化生成SO3: 2SO2(g)+O2(g)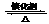 2SO3(g)。某温度下,SO2的平衡转化率(a )与体系总压强(p)的关系如图所示。根据图示回答下列问题:
2SO3(g)。某温度下,SO2的平衡转化率(a )与体系总压强(p)的关系如图所示。根据图示回答下列问题: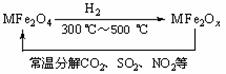 (3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M
为Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M
为Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示: