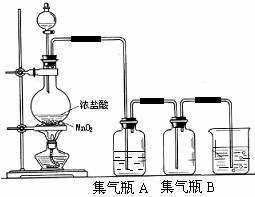
5.将淀粉溶液和淀粉酶的混合物放入玻璃纸袋中,扎好袋口,浸入流动的温水中,经相当一段时后,取袋内液体分别与碘水、新制Cu(OH)2悬浊液(加热)、浓硝酸(微热)作用,其现象依次是
|
试剂 |
A |
B |
C |
D |
|
碘水 |
显蓝色 |
显蓝色 |
无明显现象 |
无明显现象 |
|
新制Cu(OH)2(加热) |
无红色沉淀 |
红色沉淀 |
无红色沉淀 |
红色沉淀 |
|
浓硝酸(微热) |
显黄色 |
无明显现象 |
显黄色 |
无明显现象 |
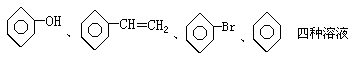 ③MnO2、FeS、CuO、C四种黑色固体
④NaCl、AlCl3、Ba(OH)2、HCl四种溶液。其中只用一种试剂(允许加热)就能将组内物质区别开的是( )
A.只有①③ B.只有①②③
C.只有①③④ D.全部
③MnO2、FeS、CuO、C四种黑色固体
④NaCl、AlCl3、Ba(OH)2、HCl四种溶液。其中只用一种试剂(允许加热)就能将组内物质区别开的是( )
A.只有①③ B.只有①②③
C.只有①③④ D.全部 ·Cr
·Cr ]O4(磁性材料铁氧体的组成)沉淀。试回答:
]O4(磁性材料铁氧体的组成)沉淀。试回答: Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O