22.(10分)(每空2分,共10分)(1) 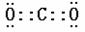 三角锥形
三角锥形
|
|||
|
|||
(2)2Mg+CO2 2MgO+C; 4NH3+5O2
4NO+6H2O
|
(3)NH4++HCO3-+2OH-+2OH NH3↑+CO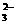 +2H2O
+2H2O
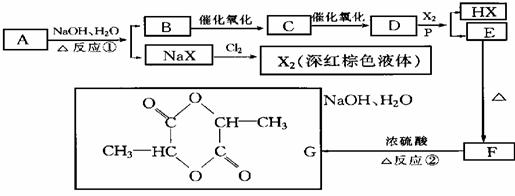
27.(12分)中学教材上有如下介绍:在氢氧化钠浓溶液中加入氧化钙,加热,制成的白色固体就是碱石灰。有两个实验小组的同学决定通过实验探究碱石灰的组成。
(1)第一小组设计方案的流程如下:

①写出n(OH-)、n(Ca2+)和n(Na+)的关系:n(Na+)=________________________。
②设n(Na+)=xmol、n(Ca2+)=ymol,请填写下表:
|
碱右灰的 可能组成 |
NaOH、CaO |
NaOH、CaO、Ca(OH)2 |
NaOH、Ca(OH)2 |
NaOH、Ca(OH)2、H2O |
|
n(Na+)和n(Ca2+) 的关系 |
40x+56y=0.4 |
|
|
|
(2)第二小组同学查得如下资料:Ca(OH)2在250℃时不分解、NaOH在580℃时不分解。他们设计了如下方案并得出相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.6g,剩余固体在580℃时继续加热至恒重,固体质量又减少了0.7g。请通过计算确定该碱石灰各成分的质量分数。
高 考 模 拟 考 试
化学参考答案
 (2)CH3CH2CH2Br+NaOH
CH3CH2CH2OH+NaBr
(2)CH3CH2CH2Br+NaOH
CH3CH2CH2OH+NaBr (或CH3CH2CH2Br+H2O+H2O
CH3CH2CH2OH+HBr)
(或CH3CH2CH2Br+H2O+H2O
CH3CH2CH2OH+HBr)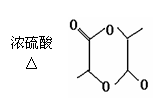
 2CH3CH2COOH +2H2O
2CH3CH2COOH +2H2O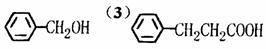
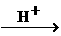 H2S
H2S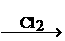 S
S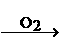 SO2
SO2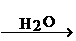 H2SO4。
H2SO4。 NH4+
NH4+ NH3
NH3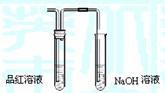 ② Fe2O3
SO3
(各2分)
② Fe2O3
SO3
(各2分) Fe2O3+SO2↑+SO3↑+14H2O(2分)
Fe2O3+SO2↑+SO3↑+14H2O(2分)