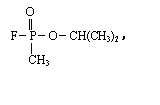4.氧族元素的氢化物的沸点如下表:
|
H2O |
H2S |
H2Se |
H2Te |
|
100℃ |
-60.75℃ |
-41.5℃ |
-1.8℃ |
下列关于氧族元素氢化物沸点高低的分析和推断中,不正确的是 ( )
A.与分子间作用力的大小无关
B.与分子间作用力的大小有关
C.水分子之间一定存在其他几种氢化物分子间所没有的特殊的分子间作用力
D.H2S、H2Se、H2Te分子间作用力随相对分子质量的增大而增大
4.(★★★★★)已知,向Zn2+溶液中滴加氨水,生成Zn(OH)2白色沉淀;但是氨水过量时,沉淀又溶解,生成了Zn(NH3)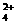 。此外,Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液中,生成ZnO
。此外,Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液中,生成ZnO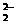 ,所以Zn(OH)2是一种两性氢氧化物。
,所以Zn(OH)2是一种两性氢氧化物。
现有4组离子,每组有2种金属离子。请各选用1种试剂,将它们两者分开,可供选用的试剂有:
A.硫酸 B.盐酸 C.硝酸 D.氢氧化钠溶液 E.氨水 请填写下表:(填写时用字母代号)
|
离子组 |
选用的试剂(代号) |
沉淀物的化学式 |
保留在溶液中的离子 |
|
(1)Zn2+和Al3+ |
|
|
|
|
(2)Zn2+和Mg2+ |
|
|
|
|
(3)Zn2+和Ba2+ |
|
|
|
|
(4)Fe3+和Al3+ |
|
|
|
 如图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁)。
如图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁)。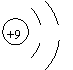
 A.F-的结构示意图:
B.乙炔的分子模型示意图:
A.F-的结构示意图:
B.乙炔的分子模型示意图: D.乙酸的结构简式:C2H4O2
D.乙酸的结构简式:C2H4O2