0 33584 33592 33598 33602 33608 33610 33614 33620 33622 33628 33634 33638 33640 33644 33650 33652 33658 33662 33664 33668 33670 33674 33676 33678 33679 33680 33682 33683 33684 33686 33688 33692 33694 33698 33700 33704 33710 33712 33718 33722 33724 33728 33734 33740 33742 33748 33752 33754 33760 33764 33770 33778 447348
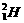 )中含有的中子数为NA
)中含有的中子数为NA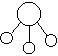 +
+
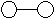
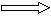
 +
+
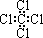 D. 臭氧的分子式O3
D. 臭氧的分子式O3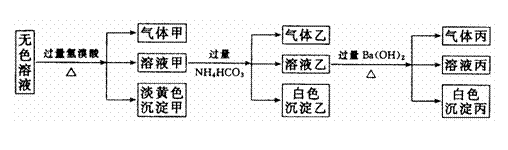 AlO2-、S2-、SO
AlO2-、S2-、SO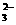 、SO
、SO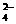 ,现取该溶液进行有关实验,实验结如下:
,现取该溶液进行有关实验,实验结如下: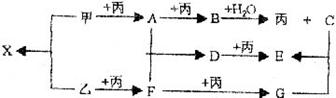 24(8分)已知甲、乙、丙常见单质,A、B、C、D、E、F、G、X均为常见的化合物;B和X的摩尔质量相同,E的式量比D的式量大16,在一定条件下,各物质的相互转化关系如下图所示:
24(8分)已知甲、乙、丙常见单质,A、B、C、D、E、F、G、X均为常见的化合物;B和X的摩尔质量相同,E的式量比D的式量大16,在一定条件下,各物质的相互转化关系如下图所示: 19某实验小组对中学课本中可生成H2的反应进行了研究,总结出四个可以生成H2的反应①Zn和盐酸
②钠和水 ③铝和氢氧化钠溶液 ④钠和无水乙醇.为点燃上述四个反应生成的氢气,他们设计了如图所示的装置:
19某实验小组对中学课本中可生成H2的反应进行了研究,总结出四个可以生成H2的反应①Zn和盐酸
②钠和水 ③铝和氢氧化钠溶液 ④钠和无水乙醇.为点燃上述四个反应生成的氢气,他们设计了如图所示的装置: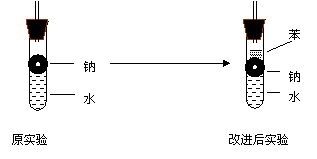 ⑷实验小组查阅钠 苯 水的密度分别是0.97g/ml 0.88 g/ml 1.00
g/ml并据此对实验进行了改进
⑷实验小组查阅钠 苯 水的密度分别是0.97g/ml 0.88 g/ml 1.00
g/ml并据此对实验进行了改进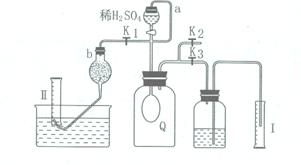 为测定可能部分变质的过氧化钠(含碳酸钠)的纯度,设计如右图所示的实验,其中Q为一开始无气体的气囊。取一定量的样品放于Q中,按图安装好实验装置,打开分液漏斗的活塞,将稀硫酸滴入气囊中充分反应(液体体积忽略不计)。
为测定可能部分变质的过氧化钠(含碳酸钠)的纯度,设计如右图所示的实验,其中Q为一开始无气体的气囊。取一定量的样品放于Q中,按图安装好实验装置,打开分液漏斗的活塞,将稀硫酸滴入气囊中充分反应(液体体积忽略不计)。