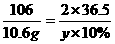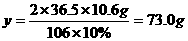3.忽视基本题型的解题方法的总结和对比,造成复分解反应的相关规律的应用经常失误。
解答关于复分解反应的试题时,要注意对以下方面的一些知识点的梳理和方法的积累:①酸碱盐的溶解性,这是涉及到判断复分解反应的发生与否、溶液中物质或离子共存问题等的解题依据;②物质除杂的原则和方法,其原则为“不增、不减、易分、复原”即:不引入新的杂质,不减少主要成分的量,操作方法简单、容易将杂质分离,如果采用化学方法将主要成分变了,要能变回来;其方法为转化法和去除法;③物质推断的题型和方法,常规的题型有:表格型、叙述型、框图型等,推断题的解答思路是:寻找突破口-分析推导-验证确认。其中寻找突破口是关键,分析推导是难点,验证确认是保证。④物质鉴别的题型和方法,常规的题型有:不用任何试剂鉴别、只用一种试剂鉴别、用多种试剂鉴别,其中只用一种试剂鉴别题型频繁出现,其方法如下表:
|
鉴别物质的特征 |
方法和实例 |
|
难溶于水的多种物质的鉴别 |
根据其酸溶性或碱溶性来确定试剂。如鉴别木炭粉、铁粉、氧化铜、三种黑色粉末,可选用盐酸或稀硫酸。 |
|
易溶于水的多种酸、碱、盐的鉴别 |
根据物质的酸碱性不同选用适当的指示剂或PH试纸加以鉴别。如盐酸、氯化钠溶液、氢氧化钠溶液的鉴别,可选用石蕊试液。 根据阳离子对应碱的溶解性、颜色、稳定性等加以鉴别。如鉴别NaCl、MgCl2、NH4Cl、FeCl3四种溶液可选用氢氧化钠溶液。 |
[基础演练]
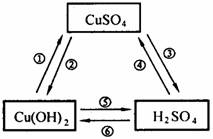
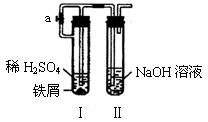
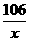 =
=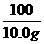 x=
x= =10.6g
=10.6g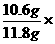 100%=89.8%
100%=89.8%