1.常见阳离子的检验
|
物质 |
检验方法 |
|
H+ |
能使紫色石蕊试液或橙色的甲基橙试液变为红色。 |
|
Na+、K+ |
用焰色反应来检验时,它们的火焰分别呈黄色、浅紫色(通过蓝色钴玻璃片观察钾离子焰色)。 |
|
Ba2+ |
能使稀H2SO4或可溶性硫酸盐溶液产生白色BaSO4沉淀,且沉淀不溶于稀HNO3。 |
|
Mg2+ |
能与NaOH溶液反应生成白色Mg(OH)2沉淀,该沉淀能溶于NH4Cl溶液。 |
|
Al3+ |
能与适量的NaOH溶液反应生成白色Al(OH)3絮状沉淀,该沉淀能溶于盐酸或过量的NaOH溶液。 |
|
Ag+ |
能与稀盐酸或可溶性盐酸盐反应,生成白色AgCl沉淀,不溶于稀HNO3,但溶于氨水,生成 [Ag(NH3)2]+。 |
|
NH4+ |
铵盐(或浓溶液)与NaOH浓溶液反应,并加热,放出使湿润的红色石蕊试纸变蓝或有刺激性气味的NH3气体。 |
|
Fe2+ |
能与少量NaOH溶液反应,开始时生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀。或向亚铁盐的溶液里加入KSCN溶液,不显红色,加入少量新制的氯水后,立即显红色。有关反应方程式为:2Fe2+ + Cl2=2Fe3+
+ 2Cl-。 |
|
Fe3+ |
能与KSCN溶液反应,变为血红色溶液;能与NaOH溶液反应,生成红褐色Fe(OH)3沉淀。 |
|
Cu2+ |
蓝色溶液(浓的CuCl2溶液显绿色)能与NaOH溶液反应,生成蓝色的
沉淀,加热后可转变为黑色的CuO沉淀。含Cu2+溶液能与Fe、Zn片等反应,在金属片上有红色的铜生成。 |
3.胶体的重要性质
①丁达尔现象:光通过胶体时所产生的光亮的通路的现象。胶体的丁达尔现象是由于胶体微粒对光线的散射而形成的,溶液无此现象,故可用此法区别溶液和溶胶。
②布朗运动:胶体粒子所作的无规则的、杂乱无章的运动。布朗运动是分子运动的体现。
③电泳现象:在外加电场的作用下,胶粒在分散剂里向阴极或阳极作定向移动的现象。工业生产中可利用电泳现象来分离提纯物质。
|
胶体微粒 |
吸附的离子 |
胶粒带的电荷 |
在电场中胶粒移动方向 |
|
金属氢氧化物、金属氧化物 |
阳离子 |
正电荷 |
阴极 |
|
非金属氧化物、金属硫化物 |
阴离子 |
负电荷 |
阳极 |
例如:在电泳实验中,Fe(OH)3胶体微粒向阴极移动,使阴极附近颜色加深,呈深红褐色;而As2S3胶体微粒向阳极移动,使阳极附近颜色加深,呈深金黄色。
④胶体的聚沉:一定条件下,使胶体粒子凝结而产生沉淀。胶体聚沉的方法主要有三种:a.加入电解质 b.加入与胶粒带相反电荷的另一种胶体 c.加热。如:制皂工业生产中的盐析,江河入海口三角洲的形成等等。
⑤渗析:依据分散系中分散质粒子的直径大小不同,利用半透膜把溶胶中的离子、分子与胶粒分离开来的方法。利用渗析可提纯胶体。
[例3](2008·湖北仙桃) Fe(OH)3胶体中常混有FeCl3和HCl。试回答有关问题:
(1) 实验室制取Fe(OH)3胶体的方法是______________________________________,用__________方法除去胶体中的浑浊;根据____________现象证明胶体已经制成。
(2) 鉴别溶液中存在Fe3+和H+的方法是_____________________________________
_________________________________________________________________________。
(3) 除去胶体中混有的FeCl3和HCl的方法是____________________________。
(4) 如何用实验方法证明胶体和Cl-两者已经分离?______ _______________ _______________________________________________________。
[解析]向沸水中滴加饱和FeCl3溶液可制得Fe(OH)3胶体;利用过滤法可分离浊液和胶体,利用渗析法可分离浊液和胶体;利用丁达尔效应可以检验胶体的存在。
[答案](1)在沸腾的蒸馏水中滴加饱和FeCl3溶液,待溶液呈红褐色,停止加热,即制得胶体 ;过滤 ;丁达尔现象
(2)滴加KSCN溶液,变红色说明有Fe3+,pH试纸检验,变红,说明有H+
(3)渗析(将胶体装入半透膜中,然后置于蒸馏水中)
(4)取半透膜外最后一次的溶液少许于试管中,加入AgNO3溶液,若无沉淀产生,证明两者已经分离。
 气溶胶--雾、云、烟
气溶胶--雾、云、烟 按分散剂状态分 液溶胶--Fe(OH)3胶体、蛋白质溶液
按分散剂状态分 液溶胶--Fe(OH)3胶体、蛋白质溶液 按分散质分 粒子胶体-分散质微粒是很多分子或离子的集合体,如Fe(OH)3胶体
按分散质分 粒子胶体-分散质微粒是很多分子或离子的集合体,如Fe(OH)3胶体
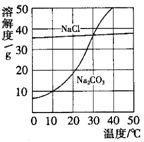 (1)当温度为10℃时,碳酸钠的溶解度为
;
(1)当温度为10℃时,碳酸钠的溶解度为
;