已知相关物质的沸点如下表:
|
物质 |
乙醛 |
乙酸 |
硅油 |
水 |
植物油 |
|
沸点 |
20.8℃ |
117.9℃ |
180℃以上 |
100℃ |
175℃ |
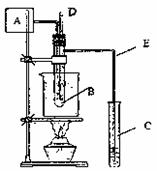
当温度计的读数为60℃-80℃时在A处鼓入空气10-15次,继续加热,最终在试管C中得到的水溶液为乙酸溶液。请回答下列问题:
(1)写出上述方法制取乙酸的化学方程式 。
(2)在烧杯中放硅油的原因是 ,为了保证实验的成功,在烧杯中也可以用 代替硅油。在鼓入空气前后 的温度计水银球的位置是:鼓入前 鼓入后: ,最后温度应控制在 。
(3)对C试管中收集到的水溶液检验的常见方法是:
① 。
② 。
③ 。
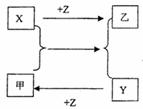
26.(B)苯甲醛在医药、染料、香料等行业有着广泛的应用。实验通过图示的流程有甲苯氧化制备苯甲醛。
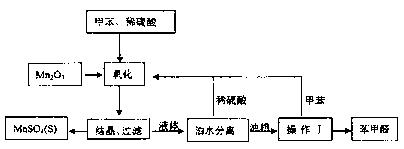
试回答下列问题:
(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是
。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需要将混合冷却,其目的是 。
(3)实验过程中需循环使用的物质分别是 、
。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是
,其原理是
。
(5)实验中发现,反应时间不同苯甲醛的产率也不同(数据见表)
|
反应时间/h |
1 |
2 |
3 |
4 |
5 |
|
苯甲醛产率/% |
76.0 |
87.5 |
83.6 |
72.5 |
64.8 |
请结合甲醛的结构,分析当反应时间过长时,苯甲醛产率下降的原因是
。
22.现有浓度为0.2摩尔/某升一元弱酸HX与浓度的0.1摩尔/升的氢氧化钠等体积混合后(忽略混合后溶液体积的变化),所得混合溶液中存在的下列关系可能正确的是( )
A.2c(Na+)=c(X-)+c(HX)=0.2mol·L-1
B.2CX-)>c(Na+)>c(H+)>c(OH-)
C.c(Na+)-c(X-)=c(H+)-c(HX)+c(OH-)
D.c(Na+)>c(X-)>c(OH-)>c(H+)
第Ⅱ卷 (共84分)
|
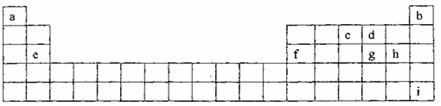
请你根据表中所给元素,回答下列问题:
(1)cdgh元素的氢化物中,沸点最高的是 (填该分子的电子式)。
(2)比较e、f单质及ef形成的合金,三者硬度由大到小的顺序 (填写名称)
(3)原子核外s电子总数比p电子总数少4个元素为 (填写元素符号),学习该元素低价氧化物的化学性质时,你可从三方面去把握;
①依据物质的类别,可知该氧化物属于 ;
②依据元素的化合价,可知该氧化物具有 ;
③将该氧化物通入 溶液中,使该溶液褪色,该氧化物具有 性。
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重大贡献的化学家莫瓦桑,你认为最先用来与F2反应制备稀有气体化合物的元素是 (填写元素符号)。
(5)用来组成酸、碱、盐三类物质至少需要的元素有 (填写表中字母)。


 一氨基酸的相对分子质量均为偶数
一氨基酸的相对分子质量均为偶数