13.(2007广东化学24)(10分)二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
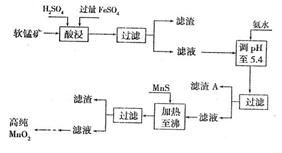
某软锰矿的主要成分是MnO2,还含Si(16.27%)、Fe(5.86%)、A1(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表。回答下列问题
|
沉淀物 |
A1(OH)2 |
Fe(OH)3 |
Fe(OH)2 |
Ma(OH)2 |
Ca(OH)2 |
|
pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
|
沉淀物 |
Zn(OH)2 |
CaS |
ZaS |
MaS |
FeS |
|
pH |
8.0 |
[≥0.42] |
≥2.5 |
≥7 |
≥7 |
(1)硫酸亚铁在酸性条件下将 MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为 。
(2)滤渣A的主要成分为 。
(3)加入MnS的目的是除去 杂质。
(4)碱性锌锰干电池中,MnO2参与的电极反应方程式为 。
(5)从废旧碱性锌锰干电池中可以回收利用的物质有 (写出两种)。
12.(2007山东理综29)(15分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
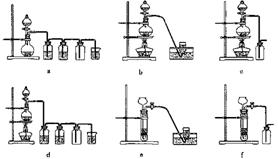
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。正极反应 负板反应 。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤 。
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
|
提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式 劣质不锈钢腐蚀的实验现象
 L
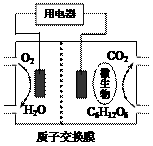
L 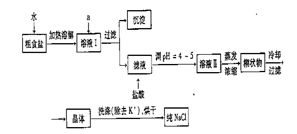 (2009·理综上海卷,11)茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中 ( )
(2009·理综上海卷,11)茫茫黑夜中,航标灯为航海员指明了方向。航标灯的电源必须长效、稳定。我国科技工作者研制出以铝合金、Pt-Fe合金网为电极材料的海水电池。在这种电池中 ( )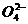 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下: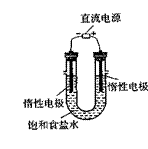 (3)电解饱和食盐水的装置如图所示,若收集的 H2为2 L ,则同样条件下收集的Cl2 (填“>”、“=”或“<”
(3)电解饱和食盐水的装置如图所示,若收集的 H2为2 L ,则同样条件下收集的Cl2 (填“>”、“=”或“<” 2 L,原因是 。装 置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为
。
2 L,原因是 。装 置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为
。
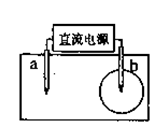 圆为白色,外圆呈浅红色。则下列说法错误的是
( )
圆为白色,外圆呈浅红色。则下列说法错误的是
( )