3、NO与O2分别通入水中
关系式:4NO+3O2+H2O=4HNO3
讨论如下:
|
NO与O2的体积比 |
发生的化学反应 |
剩余气体 |
|
=4:3 |
4NO+3O2+H2O=4HNO3 |
无 |
|
<4:3 |
4NO+3O2+H2O=4HNO3 |
O2 |
|
>4:3 |
4NO+3O2+H2O=4HNO3 |
NO |
例3.一定条件下,将等体积的NO和O2混合于一试管中,然后将试管倒立于盛有水的水槽中,充分反应后剩余气体的体积与原混合气体的体积之比是多少?
解析: 因为混合气体中NO和O2的体积比<4:3,则剩余气体为O2
设混合气体中NO 的体积为x,则O2的体积也为x
4NO+3O2+H2O=4HNO3
4 3
x y
4/ x =3 / y 解得:y=3x/4
剩余的O2为x-3x/4=x/4
它与原混合气体的体积比为x/4:2x=1:8
2、NO2和O2 的混合气体与水的反应
关系式:4NO2+O2+H2O=4HNO3
将(2)×2-(1)得到,目的:消去中间产物NO)
讨论如下:
|
NO2与O2的体积比 |
发生的化学反应 |
剩余气体 |
|
=4:1 |
4NO2+O2+H2O=4HNO3 |
无 |
|
<4:1 |
4NO2+O2+H2O=4HNO3 |
O2 |
|
>4:1 |
4NO2+O2+H2O=4HNO3 3NO2+H2O=2H2NO3+NO |
NO |
例2.将充满NO2和O2的混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的一半处停止了,则原混合气体中NO2和O2的体积比是多少?
解析:NO2和O2的体积比不等于4:1,则需讨论NO2和O2分别过量时的两种情况
设混合气体的体积为1,混合气体中NO2的体积为x,则O2为(1- x)
(1)假定原混合气体中V(NO2):(O2)<4:1
4NO2+O2+H2O=4HNO3
4 1
x y
4/x=1/y 解得y=x/4
剩余的O2:(1-x)-x/4=1/2 解得x=2/5
V(NO2):V(O2)=2/5:(1-2/5)=2:3
(2) 假定原混合气体中V(NO2):V(O2)>4:1
4NO2+O2+H2O=4HNO3
4 1
y (1-x)
4/ y =1/(1-x) 解得:y=4(1-x)
暂时剩余NO2:1-[4(1-x)+(1-x)]=5x-4
由反应式:3NO2+H2O=2H2NO3+NO可知
最后剩余NO :(5x-4)/3
由(5x-4)/3=1/2得 x=11/10(不合题意,舍去)
小结: NO2和O2的混合气体与水反应时,当剩余气体的体积大于原混合气体体积的1/3时,只有一个条件:V(NO2):V(O2)>4:1(此结论由同学们自行证明)
2.氮气的性质
(1)氮气的物理性质:无色无味,不溶于水比空气略轻的气体。
(2)氮气的化学性质:
 分子中N≡N非常牢固,通常情况下不易与其他物质反应。
分子中N≡N非常牢固,通常情况下不易与其他物质反应。
N2 与氢气反应生成NH3(高温高压铁触媒)
与氧气在放电条件下生成NO
与活泼金属反应 3Mg+N2 Mg3N2
(3)氮气的用途:
工业上合成氨制硝酸;用作保护气,用于:焊接金属、填充灯泡、保鲜食品;医学上用于冷冻麻醉;高科技中用液氮制造低温环境等。
3 .磷的同素异形体:白磷和红磷
.磷的同素异形体:白磷和红磷
|
名称 |
白磷 |
红磷 |
|
分子结构 |
分子式P4、正四面体型、键角60° |
分子晶体、结构复杂 |
|
颜色状态 |
白色或黄色固体 |
暗红色粉末或固体 |
|
溶解性 |
不溶于水,易溶于CS2 |
不溶于水,不溶于CS2 |
|
毒性 |
剧毒 |
无毒 |
|
着火点 |
40℃ |
240℃ |
|
保存方法 |
保存在水中 |
密封 |
|
相互转化 |
 |
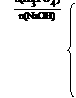 =1∶1时生成NaH2PO4
=1∶1时生成NaH2PO4
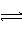 NO2+2KI=2KNO2+I2(NO2能使湿润的淀粉KI试纸为蓝)
NO2+2KI=2KNO2+I2(NO2能使湿润的淀粉KI试纸为蓝) 4P+5O2 2P2O5
4P+5O2 2P2O5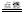 2P+3Cl2 2PCl3(l)
2P+3Cl2 2PCl3(l)