摘要:1.氮族元素最外层电子都是5个.主要显+5.+3.-3价.本族元素形成的+3.-3价化合物中其原子已达到稳定结构.如NH3.PCl3.BiCl3.Mg3N2.
网址:http://m.1010jiajiao.com/timu3_id_51284[举报]
A、B、C、D、E为5种短周期元素,且原子序数依次增大.A的原子半径最小;B的电子总数与其最外层电子数之比为3:2;C的最高价氧化物对应水化物与其简单氢化物反应生成一种盐类物质甲.A、E同主族,A、B、C、E都能分别与D形成原子个数比不同的常见化合物.请回答下列问题:
(1)B在周期表中位于第 族,甲的名称是 .
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为 .在微电子工业中,M的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为 .
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分.现取13.0g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6.72L)和一种固体单质,则乙的化学式是 .
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.汽车内燃机工作时引起反应:C2(g)+D2(g)?2CD(g),是导致汽车尾气中含有CD的原因之一.T℃时,向容积为2L的密闭容器中充入10molC2与5molD2,达到平衡后CD的物质的量为2mol,则T℃时该反应的平衡常数K= (计算结果保留两位有效数字).在其他条件不变的情况下,再通入10molC2与5moD2,达到平衡常数时C2的转化率将 (填“增大”、“减小”或“不变”,下同),CD的平衡浓度将 .
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ?mol-1
△H2= .
查看习题详情和答案>>
(1)B在周期表中位于第
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分.现取13.0g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6.72L)和一种固体单质,则乙的化学式是
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物.汽车内燃机工作时引起反应:C2(g)+D2(g)?2CD(g),是导致汽车尾气中含有CD的原因之一.T℃时,向容积为2L的密闭容器中充入10molC2与5molD2,达到平衡后CD的物质的量为2mol,则T℃时该反应的平衡常数K=
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染.
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2(g)△H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H3=-867kJ?mol-1
△H2=
A、B、C、D、E为5种短周期元素,且原子序数依次增大。A的原子半径最小;B的电子总数与其最外层电子数之比为3:2;C的最高价氧化物对应水化物与其简单氢化物反应生成一种盐类物质甲。A、E同主族,A、B、C、E都能分别与D形成原子个数比不同的常见化合物。请回答下列问题:
(1)B在周期表中位于第______族,甲的名称是___________。
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为___________。在微电子工业中,M的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为________________。
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分。现取13.0 g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6. 72L)和一种同体单质,则乙的化学式是___________。
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。汽车内燃机工作时引起反应:C2(g)+D2(g)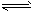 2CD(g),是导致 汽车尾气中含有CD的原因之一。T℃时,向容积为2L的密闭容器中充入10 mol C2与5 mol D2,达到平衡后CD的物质的量为2 mol,则T℃时该反应的平衡常数K=
2CD(g),是导致 汽车尾气中含有CD的原因之一。T℃时,向容积为2L的密闭容器中充入10 mol C2与5 mol D2,达到平衡后CD的物质的量为2 mol,则T℃时该反应的平衡常数K=
____________(计算结果保留两位有效数字)。在其他条件不变的情况下,再通入10mol C2与5 mol D2,达到新平衡时C2的转化率将____(填“增大”“减小”或“不变”,下同),CD的平衡浓度将____。
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2O(g) △H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3=-867 kJ/mol
△H2=___________。
查看习题详情和答案>>
(1)B在周期表中位于第______族,甲的名称是___________。
(2)A、C两元素按原子数目比3:1和2:1构成分子M和N,N的电子式为___________。在微电子工业中,M的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为________________。
(3)由C、E组成的化合物乙是汽车安全气囊中的一种成分。现取13.0 g乙,加热使其完全分解,生成一种气体单质(标准状况下的体积为6. 72L)和一种同体单质,则乙的化学式是___________。
(4)近年来太原市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。汽车内燃机工作时引起反应:C2(g)+D2(g)
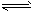 2CD(g),是导致 汽车尾气中含有CD的原因之一。T℃时,向容积为2L的密闭容器中充入10 mol C2与5 mol D2,达到平衡后CD的物质的量为2 mol,则T℃时该反应的平衡常数K=
2CD(g),是导致 汽车尾气中含有CD的原因之一。T℃时,向容积为2L的密闭容器中充入10 mol C2与5 mol D2,达到平衡后CD的物质的量为2 mol,则T℃时该反应的平衡常数K=____________(计算结果保留两位有效数字)。在其他条件不变的情况下,再通入10mol C2与5 mol D2,达到新平衡时C2的转化率将____(填“增大”“减小”或“不变”,下同),CD的平衡浓度将____。
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+4NO(g)=CO2(g)+2H2O(g)+2N2O(g) △H2
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H3=-867 kJ/mol
△H2=___________。
氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。含氮元素的化合物在工业生产和国防建设中都有广泛的应用。
(1)氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。PH3分子的空间构型为 ,是 分子。(填极性或非极性)
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)
a.NH3比PH3稳定性强
b.硝酸显强氧化性,磷酸不显强氧化性
c.氮气与氢气能直接化合,磷与氢气很难直接化合
d.氮气常温是气体,磷单质是固体
亚硝酸盐是食品添加剂中急性毒性较强的物质之一,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。
(3)亚硝酸钠溶液滴加到K2Cr2O7酸性溶液中,溶液由橙色变为绿色,反应如下,补上缺项物质并配平:
Cr2O72-+ NO2-+ → Cr3+ + NO3-+
(4)上题反应中每消耗0.6mol NO2-,转移电子数为 。
(5)氮氧化物(NO和NO2)污染环境。若用Na2CO3溶液吸收NO2可生成CO2,9.2gNO2和Na2CO3溶液完全反应时转移电子0.1 mol,则反应的离子方程式为 。
氮元素广泛存在于自然界中,对人类生命和生活具有重要意义。含氮元素的化合物在工业生产和国防建设中都有广泛的应用。
(1)氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。PH3分子的空间构型为 ,是 分子。(填极性或非极性)
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)
a.NH3比PH3稳定性强
b.硝酸显强氧化性,磷酸不显强氧化性
c.氮气与氢气能直接化合,磷与氢气很难直接化合
d.氮气常温是气体,磷单质是固体
亚硝酸盐是食品添加剂中急性毒性较强的物质之一,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。
(3)亚硝酸钠溶液滴加到K2Cr2O7酸性溶液中,溶液由橙色变为绿色,反应如下,补上缺项物质并配平:
Cr2O72-+ NO2-+ → Cr3+ + NO3-+
(4)上题反应中每消耗0.6mol NO2-,转移电子数为 。
(5)氮氧化物(NO和NO2)污染环境。若用Na2CO3溶液吸收NO2可生成CO2,9.2gNO2和Na2CO3溶液完全反应时转移电子0.1 mol,则反应的离子方程式为 。
(1)氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。PH3分子的空间构型为 ,是 分子。(填极性或非极性)
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)
a.NH3比PH3稳定性强
b.硝酸显强氧化性,磷酸不显强氧化性
c.氮气与氢气能直接化合,磷与氢气很难直接化合
d.氮气常温是气体,磷单质是固体
亚硝酸盐是食品添加剂中急性毒性较强的物质之一,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。
(3)亚硝酸钠溶液滴加到K2Cr2O7酸性溶液中,溶液由橙色变为绿色,反应如下,补上缺项物质并配平:
Cr2O72-+ NO2-+ → Cr3+ + NO3-+
(4)上题反应中每消耗0.6mol NO2-,转移电子数为 。
(5)氮氧化物(NO和NO2)污染环境。若用Na2CO3溶液吸收NO2可生成CO2,9.2gNO2和Na2CO3溶液完全反应时转移电子0.1 mol,则反应的离子方程式为 。
有A、B、C、D、E、F六种元素.A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化物;D与B可形成离子化合物,其晶胞结构如右图1所示.请回答下列问题.
(1)E元素原子基态时的外围电子排布式为
(2)A2F分子中F原子的杂化类型是
(3)CA3极易溶于水,其原因是
(4)从晶胞结构图1中可以看出,D跟B形成的离子化合物的电子式为
 ;该离子化合物晶体的密度为ρ(g?cm-3).,则晶胞的体积是
;该离子化合物晶体的密度为ρ(g?cm-3).,则晶胞的体积是
(只要求列出算式).
(5)BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为
(6)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为

查看习题详情和答案>>
(1)E元素原子基态时的外围电子排布式为
3d104s1
3d104s1
.(2)A2F分子中F原子的杂化类型是
sp3
sp3
,F的气态氧化物FO3分子的键角为60°
60°
.(3)CA3极易溶于水,其原因是
与水分子之间形成氢键,且二者都是极性分子
与水分子之间形成氢键,且二者都是极性分子
,试判断CA3溶于水后,形成CA3?H2O的最合理结构为b
b
(选填字母).(4)从晶胞结构图1中可以看出,D跟B形成的离子化合物的电子式为


| ||
| ρg?cm-3 |
| ||
| ρg?cm-3 |
(5)BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为
正四面体
正四面体
;(6)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
共价键
共价键
,层间作用力为范德华力
范德华力
.