24.(8分)⑴20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理
论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的
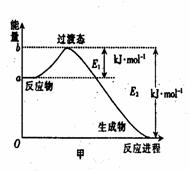
过渡态。图甲是1mol白磷(P4)和足量O2反应生成P4O10过程中能量变化示意图,请写出白磷(P4)
和O2反应生成P4O10的热化学方程式:
(△H用含E1和E2的代数式表示,其中E1、E2均大于0)。
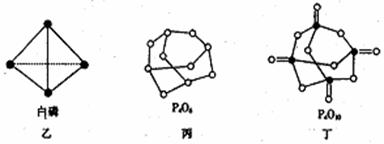
⑵白磷(图乙)是正四面体构型的分子,当与氧气作用形成P4O6时,相当于每两个磷原子之间
插入一个氧原子(如图丙)。当形成P4O10时,相当于在P4O6的分子中每个磷原子又以双键结合一个
氧原子(如图丁)。请在图丙的示意图中把磷原子用钢笔或铅笔把磷原子涂黑。
⑶进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关。键能可以简
单的理解为断开1mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
|
化学键 |
P-P |
P-O |
O=O |
P=O |
|
键能/ kJ·mol-1 |
198 |
360 |
498 |
X |
已知白磷(P4)的燃烧热为2982kJ/mol,
白磷完全燃烧的产物结构如图丁所示,则上表
中x=_________。
⑷写出1 mol P4与O2反应生成固态P4O6的反应热△H=_____________。
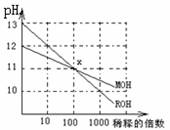 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示,下列叙述中正确的是
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示,下列叙述中正确的是

 R-CN RCOOH, R-Cl+CN- R-CN+Cl-(R为烃基)
R-CN RCOOH, R-Cl+CN- R-CN+Cl-(R为烃基)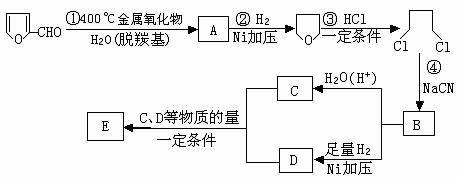
 (10分)已知:①R-
-; ;②苯环上原有的取代基对新导入的取代基进
(10分)已知:①R-
-; ;②苯环上原有的取代基对新导入的取代基进
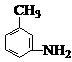 的所有原子 (填“是”或“不是”)在同一平面上。
的所有原子 (填“是”或“不是”)在同一平面上。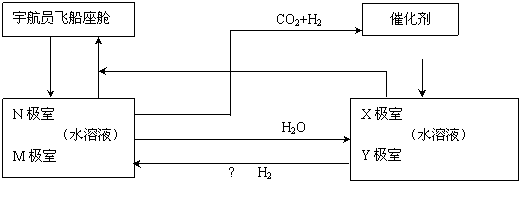 方法二:有的科学家根据电解原理设计了飞船内空气更新实验系统,该系统结构示意图如下:
方法二:有的科学家根据电解原理设计了飞船内空气更新实验系统,该系统结构示意图如下: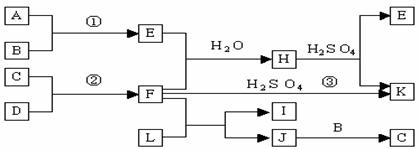 成,其相对分子质量为32。请按要求填空:
成,其相对分子质量为32。请按要求填空:
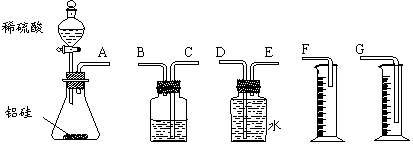 的反应测定通常状况(约20℃,1atm)下气体摩尔体积的方法。
的反应测定通常状况(约20℃,1atm)下气体摩尔体积的方法。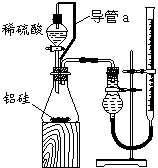 在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。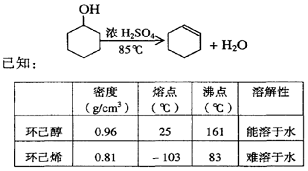
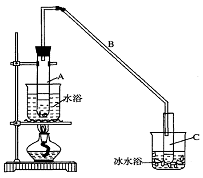
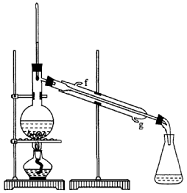 ②再将环己烯按右图装置蒸馏,冷却水从____口进入。蒸馏时要加入生石灰,目的是 。
②再将环己烯按右图装置蒸馏,冷却水从____口进入。蒸馏时要加入生石灰,目的是 。 体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验: