5.将铁、铝、硅的混合物分为等质量的两份,一份跟足量的NaOH溶液反应,另一份跟足量稀H2SO4反应,最终产生的H2一样多,则铁与硅物质的量之比为( )
A.2∶1 B.4∶1 C.1∶1 D.3∶1
22.(10分)NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:
Na2CO3+nH2O=Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管已部分变质的NaHCO3样品A 9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(不考虑CO2气体在水中的溶解)
|
盐酸体积(mL) |
8 |
15 |
20 |
50 |
x |
120 |
150 |
|
生成CO2体积(mL) |
0 |
112 |
224 |
896 |
2240 |
2240 |
2240 |
试求:
(1)当加入盐酸后,生成CO2体积不再增加时,x的最小值为 。
(2)未变质前NaHCO3的质量。
(3)部分变质后样品A中的成分及各成分的物质的量。
20. (12分)同学们利用右图装置探究SO2与Na2O2的反应。
(12分)同学们利用右图装置探究SO2与Na2O2的反应。
(1)同学们认为该反应类似CO2与Na2O2的反应,有氧气生成,当通入气体后,如果把带火星的木条伸到导管口,预期现象为带火星的木条复燃。可是,当他们把带火星的木条伸到导管口后,木条并没有复燃,你分析其原因是 ,改进的方法是 。
(2)反应完毕后,硬质玻璃管中的固体变为白色。大家认为固体成分有多种可能:
假设Ⅰ:全部为Na2SO3; 假设Ⅱ:为Na2SO3和Na2O2 的混合物;
假设Ⅲ:全部为 ; 假设Ⅳ:为Na2SO3 和Na2SO4的混合物;
假设Ⅴ:为Na2O2和Na2SO4的混合物。
假设Ⅲ、Ⅳ、Ⅴ的共同理由是 。
(3)现有下列实验用品:几支试管、带胶塞的导管(单孔)、滴管、药匙、品红溶液、蒸馏水、Ba(NO3)2溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝酸、浓硫酸、浓盐酸、浓硝酸,请你从中选出合适的用品对“假设Ⅳ”进行验证,完成下表(可以不填满):
|
实验步骤编号 |
实验操作 |
预期现象和结论 |
|
① |
,用药匙取少量白色固体于试管中。 |
 |
|
② |
向①的试管中加入
,塞紧带导管的胶塞,并将导管
。 |
|
|
③ |
|
|
|
④ |
|
|
 )
)
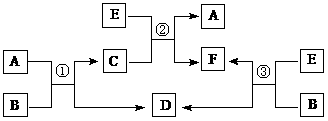
 (1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是__________________。
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是__________________。