0 42468 42476 42482 42486 42492 42494 42498 42504 42506 42512 42518 42522 42524 42528 42534 42536 42542 42546 42548 42552 42554 42558 42560 42562 42563 42564 42566 42567 42568 42570 42572 42576 42578 42582 42584 42588 42594 42596 42602 42606 42608 42612 42618 42624 42626 42632 42636 42638 42644 42648 42654 42662 447348
 (1)As的核外电子排布式为 。
(1)As的核外电子排布式为 。
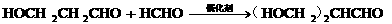 ……
……
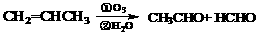
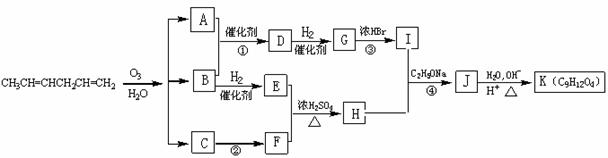
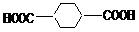 的合成路线图(无机原料任选)。
的合成路线图(无机原料任选)。
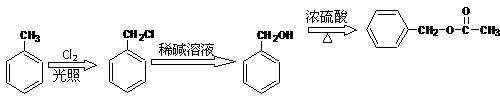
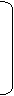
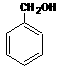
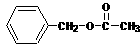

 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。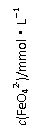

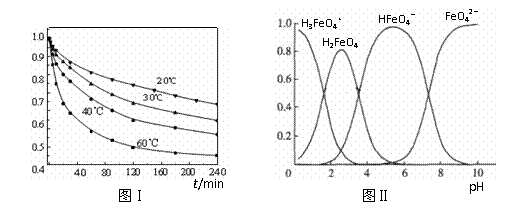

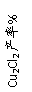
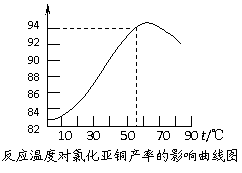 ⑵
反应②的离子方程式是
。
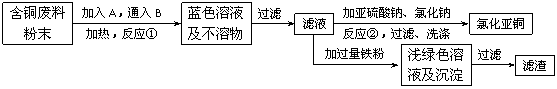
⑵
反应②的离子方程式是
。 I3–,故标准I2溶液应配成I2的KI溶液)进行滴,原理如下:
I3–,故标准I2溶液应配成I2的KI溶液)进行滴,原理如下: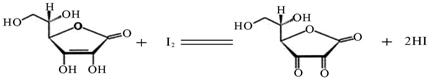
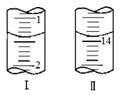 A.0.1 mol·L-1 CH3COOH
B.0.1
mol·L-1 HNO3
A.0.1 mol·L-1 CH3COOH
B.0.1
mol·L-1 HNO3