0 39937 39945 39951 39955 39961 39963 39967 39973 39975 39981 39987 39991 39993 39997 40003 40005 40011 40015 40017 40021 40023 40027 40029 40031 40032 40033 40035 40036 40037 40039 40041 40045 40047 40051 40053 40057 40063 40065 40071 40075 40077 40081 40087 40093 40095 40101 40105 40107 40113 40117 40123 40131 447348
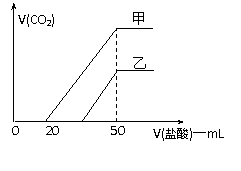 (1)NaOH溶液的物质的量浓度为 ▲ 。
(1)NaOH溶液的物质的量浓度为 ▲ 。
 (12分)已知2SO2 (g)+ O2(g) 2SO3(g) △H =-196kJ·mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:
(12分)已知2SO2 (g)+ O2(g) 2SO3(g) △H =-196kJ·mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡。如下图所示: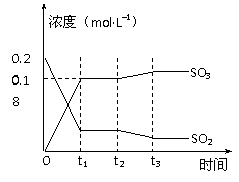
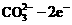 = H2O+CO2。现以该电池为电源对粗铜进行精炼。则下列推断正确的是
= H2O+CO2。现以该电池为电源对粗铜进行精炼。则下列推断正确的是 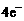 =
= 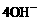 B.粗铜应该与电池中通H2的一极相连
B.粗铜应该与电池中通H2的一极相连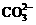 向正极移动
向正极移动