0 39573 39581 39587 39591 39597 39599 39603 39609 39611 39617 39623 39627 39629 39633 39639 39641 39647 39651 39653 39657 39659 39663 39665 39667 39668 39669 39671 39672 39673 39675 39677 39681 39683 39687 39689 39693 39699 39701 39707 39711 39713 39717 39723 39729 39731 39737 39741 39743 39749 39753 39759 39767 447348
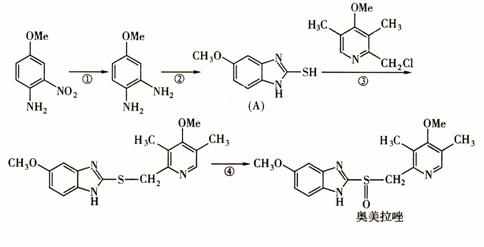
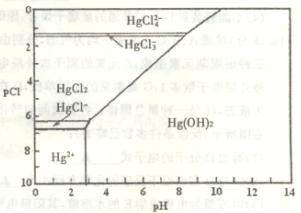 水体中二价汞离子可以与多种阴离子结合成不同的存在形态。水溶液中二价汞主要存在形态与
水体中二价汞离子可以与多种阴离子结合成不同的存在形态。水溶液中二价汞主要存在形态与 、
、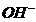 的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=一lgc(
的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=一lgc(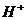 ),pCl=一lgc(
),pCl=一lgc(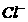 的浓度大于0.1mol/L) 中汞元素的主要存在形态是
。
的浓度大于0.1mol/L) 中汞元素的主要存在形态是
。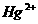 的废水。反应的离子方程式为
。
的废水。反应的离子方程式为
。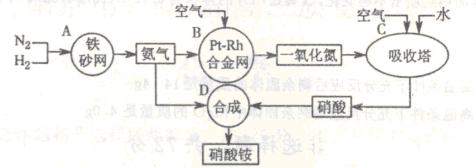
 2NH3(g) △H=一92 kJ/mol。
2NH3(g) △H=一92 kJ/mol。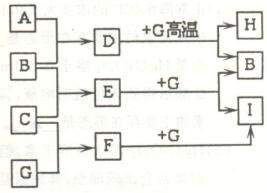 三种短周期元素组成;Z元素的原子次外层电子数比最外层电子数多1;G是常见的金属单质,D在常温下为液态,H是一种黑色固体。各物质间的转化关系如右图所示(反应条件多数已略去);
三种短周期元素组成;Z元素的原子次外层电子数比最外层电子数多1;G是常见的金属单质,D在常温下为液态,H是一种黑色固体。各物质间的转化关系如右图所示(反应条件多数已略去);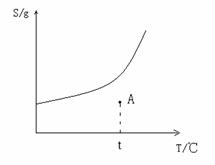 为了保证溶液达到饱和,实验操作是_______________________。 如果实验过程中把蒸发皿放在空气中冷却,没有在干燥器中冷却,会造成实验结果________(“偏高”、“偏低”、“不变”);使用温度计时仰视温度计刻度读数,会造成实验结果________(“偏高”、“偏低”、“不变”)。
为了保证溶液达到饱和,实验操作是_______________________。 如果实验过程中把蒸发皿放在空气中冷却,没有在干燥器中冷却,会造成实验结果________(“偏高”、“偏低”、“不变”);使用温度计时仰视温度计刻度读数,会造成实验结果________(“偏高”、“偏低”、“不变”)。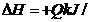 mol(Q>0)
mol(Q>0)