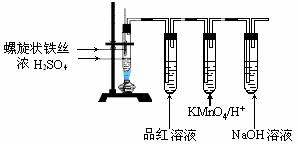
25.(14分)由CO2、H2O(g)组成的混合气体共a mol,其中CO2的物质的量分数为x。将该混合气体缓慢通过装有1mol Na2O2的真空管,充分反应后,维持1.01×105Pa,120℃收集所得气体,冷却、称量,真空管中固体质量增加y g。
(1)若a=1,则y=________ ____(用含x代数式表示)。
(2)若a=2,x=0.3时,y=_____________。
(3)若a=2,试讨论:x取值不同时,反应后所得气体成份及y的表达式(不一定填满)。
|
x的取值范围 |
反应后所得气体成份 |
y的表达式 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
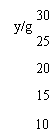 (4)若a=1.25,试作图表示y与x的关系(关键点要标明数据)。
(4)若a=1.25,试作图表示y与x的关系(关键点要标明数据)。
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|
22.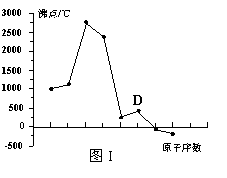 (8分)原子序数依次增大的A、B、C、D四种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多,D所在周期的各元素单质沸点变化如图I(原子序数按递增顺序连续排列)。B、C、D三种元素均能与A形成等电子的三种分子,且化合物中各原子的个数比为:
(8分)原子序数依次增大的A、B、C、D四种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多,D所在周期的各元素单质沸点变化如图I(原子序数按递增顺序连续排列)。B、C、D三种元素均能与A形成等电子的三种分子,且化合物中各原子的个数比为:
|
化合物 |
甲 |
乙 |
丙 |
|
原子个数比 |
B∶A=1∶3 |
C∶A=1∶2 |
D∶A=1∶2 |
⑴元素D在元素周期中的位置 。
⑵B、C形成的一种化合物X是一种原子晶体,晶体中B、C原子均达到稳定结构,则X的化学式为 ;X的熔点 金刚石(填“大于”、“等于”或“小于”)。
⑶写出图I中沸点最高的单质与NaOH溶液反应的离子方程式 。
20.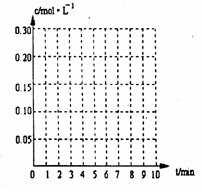 (8分)在20L恒容的密闭容器中,加入3mo1SO3(g)和lmo1氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.06 mol·L-1,当反应到8min时,反应到达平衡,此时三氧化硫浓度c(SO3)=
a mol·L-1。
(8分)在20L恒容的密闭容器中,加入3mo1SO3(g)和lmo1氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.06 mol·L-1,当反应到8min时,反应到达平衡,此时三氧化硫浓度c(SO3)=
a mol·L-1。
(1)0min-4min内生成O2平均速率v(O2)= mol·L-1·min-1;
(2)达到平衡时c(O2)=c(SO2),则a= mol·L-1,在下列坐标系中作出0min-8min及之后SO2、O2、SO3浓度随时间变化曲线.
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于a mol·L-1的是 。
|
|
A |
B |
C |
D |
|
SO3 |
1mol |
3mol |
3mol |
0mol |
|
SO2 |
2mol |
1.5mol |
0mol |
6mol |
|
O2 |
2mol |
1mol |
0mol |
5mol |
 (1)若A、D的组成元素同主族:
(1)若A、D的组成元素同主族: