25.(2009年安徽省宣城六中与奋飞学校联考)
比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因素,其中推理不合理的是( )
|
序号 |
化学反应事实 |
影响化学反应的因素 |
|
A |
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 |
反应物浓度 |
|
B |
碳在常温下不与氧气发生反应,而在高温时能与氧气反应 |
反应温度 |
|
C |
水要在通电的条件才能分解,而双氧水只要加入二氧化锰就迅速分解 |
催化剂 |
|
D |
铜片在空气中很难燃烧,钠米铜粉在空气中较易燃烧 |
反应物的接触面积 |
22.(天津市2009年中考化学冲刺模拟题十)
某校九年级(1)、(2)两班同学做常见酸和碱与指示剂反应的实验,使用的试剂如图所示,
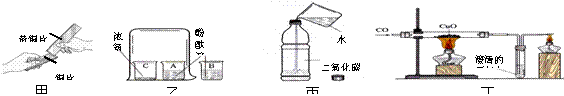
实验后废液分别集中到废液缸中。某研究小组对此废液进行了检测,结果如下表:
|
废液来源 |
检测方法 |
观察到的现象 |
|
(1)班 |
观察废液颜色 |
废液呈无色 |
|
(2)班 |
观察废液颜色 |
废液呈红色 |
请你根据以上实验现象判断,下列对该废液成分的说法中.错误的是 ( )
A.(1)班实验后的废液中可能含有盐酸 B.(1)班废液中一定含有的物质只有氯化钠
C.(2)班实验后的废液成分中肯定没有盐酸 D.(2)班实验后的废液中可能含有氢氧化钠
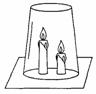 烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的房间逃离时,下列做法中不正确的是
烛后熄灭,同时还观察到茶杯内壁变黑。由此我们可以得到启发:从着火燃烧的房间逃离时,下列做法中不正确的是 是在工业上制取硫酸铜不是直接利用浓硫酸与铜反应,而是将铜屑在空气中加热氧化,然
是在工业上制取硫酸铜不是直接利用浓硫酸与铜反应,而是将铜屑在空气中加热氧化,然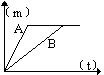 (1)曲线A表示的是 (填铁或锌)跟稀硫酸反应的情况。
(1)曲线A表示的是 (填铁或锌)跟稀硫酸反应的情况。