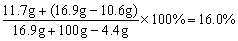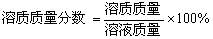(三)计算题:
1.为了给水果消毒,某同学要把30g15%的KMnO4溶液稀释成0.3%的溶液,需加水多少克?
2.将9gKNO3完全溶于21g水中,并将其均分为三份,计算:(1)取一份,其中溶质质量分数是多少?(2)取一份,使其溶质质量分数增大一倍,需加入KNO3多少克?(3)取一份,欲使其溶质质量分数减小一半,需加水多少克?
3.t℃时,4.8g镁与一定量的稀盐酸恰好完全反应,所得溶液溶质质量分数为25%.求所用盐酸中氯化氢的质量分数.
4.取22.2g石灰石样品,放入盛有126g稀盐酸的烧杯中,石灰石中的CaCO3与盐酸恰好完全反应(杂质不反应,也不溶解),烧杯内物质质量变为139.4g.求反应后所得溶液中溶质的质量分数.
5.常温下,将18.9gKCl和K2CO3的混合物溶于149g水中,向其中加入36.5g稀盐酸,恰好完全反应,得到200g不饱和溶液.求反应后所得溶液中溶质的质量分数.
6.将10g不纯的MgCl2样品(杂质不溶于水),放入50g水中,充分搅拌,待样品中MgCl2全部溶解后过滤.将所得滤液与63.3gNaOH溶液恰好完全反应,生成5.8g白色沉淀.
求:(1)样品中MgCl2的质量
(2)反应后所得溶液中溶质的质量分数
7.甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
|
|
甲 |
乙 |
丙 |
|
金属混合物质量(g) |
10 |
10 |
20 |
|
稀硫酸质量(g) |
100 |
120 |
100 |
|
反应后,过滤得干燥固体质量(g) |
2 |
2 |
12 |
计算:(1)金属混合物中铁的质量分数;
(2)甲制得硫酸亚铁质量;
(3)该稀硫酸中溶质的质量分数.
 10%的NaOH溶液,混合后溶液中NaOH质量分数为____.
10%的NaOH溶液,混合后溶液中NaOH质量分数为____.
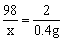 x=19.6g
x=19.6g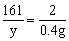 y=32.2g
y=32.2g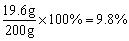
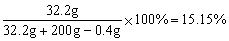
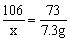 x=10.6g
x=10.6g 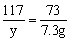 y=11.7g
y=11.7g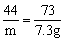 m=4.4g
m=4.4g