9. 有4组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如下表所示:
|
第一组 |
He
-268.8 |
(a) -249.5 |
Ar
-185.8 |
Kr
-151.7 |
|
第二组 |
F2 -187.0 |
Cl2 -33.6 |
(b)
58.7 |
I2 184.0 |
|
第三组 |
(c)
19.4 |
HCl
-84.0 |
HBr
-67.0 |
HI
-35.3 |
|
第四组 |
H2O
|
H2S |
(d) |
H2Te
|
下列各项判断正确的是
A、abc的化学式分别为Ne2、Br2、HF
B、第三组与第四组相比较,化合物的稳定顺序为:HBr>d
C、第三组物质溶于水后,溶液的酸性c最强
D、第四组物质中H2Te的沸点最高
8.键能的大小可用于估算化学反应的反应热(△H ),已知
|
化 学 键 |
H-H |
Cl-Cl |
H-Cl |
|
键能 |
436kJ·mol-1 |
243kJ·mol-1 |
431kJ·mol-1 |
则下列热化学方程式不正确
A.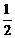 H2(g)+
H2(g)+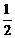 Cl2(g)=HCl(g);△H =-91.5 kJ·mol-1
Cl2(g)=HCl(g);△H =-91.5 kJ·mol-1
B. H2(g)+Cl2(g)=2HCl(g);△H =-183 kJ·mol-1
C.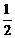 H2(g)+
H2(g)+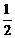 Cl2(g)=HCl(g);△H =+91.5 kJ·mol-1
Cl2(g)=HCl(g);△H =+91.5 kJ·mol-1
D.2HCl(g)=H2(g)+Cl2(g);△H =+183 kJ·mol-1
5.根据下表中给出几种氯化物的熔点和沸点,判断下列说法中不正确的是
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
单质B |
|
熔点(℃) |
801 |
714 |
190 |
-70 |
2300 |
|
沸点(℃) |
1413 |
1412 |
180 |
57 |
2500 |
A.SiCl4是分子晶体 B.单质B可能是原子晶体
C.AlCl3在加热时能升华 D.NaCl比MgCl2更容易熔化
 2C(g)+D(g),下列物理量不能确定达到平衡状态的是
2C(g)+D(g),下列物理量不能确定达到平衡状态的是 ,它与石墨互为
,它与石墨互为