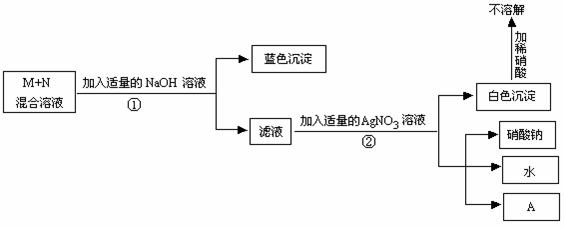
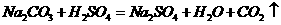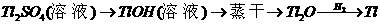25、某校化学课外活动小组研究外界条件对水中氧气含量的影响。他们利用仪器测得以下数据:
表1 某日的不同时间,长有水中植物的人工湖的水样
|
时 间 |
6:30 |
11:30 |
16:30 |
20:30 |
|
气温(℃) |
25 |
28 |
31 |
27 |
|
水中氧气的含量(mg/L) |
7.0 |
10.2 |
12.7 |
6.8 |
表2 某日同一时间,相距不远四个地点的水样
|
地点 |
造纸厂的排污口 |
菜市场的下水道 |
家中自来水 |
生长着植物的人工湖 |
|
水中氧气的含量(mg/L) |
0.2 |
1.2 |
5.0 |
11.8 |
请回答下列问题:
(1)在其它条件相同的情况下,随着温度的 (填“升高”或“降低”),氧气在水中的溶解度 (填“增大”或“减小”)
(2)分析表中的数据,可得出的结论是 。
(3)为了验证结论,进行了如右图所示的实验:
①实验要通入1种气体,这种气体是 ;
②试管内收集到的气体可用 来检验;
③欲达到该实验的目的,装置必须放在有 的环境中。
(4)若在家中饲养金鱼,提出给水增加氧气含量的两种方法:
① ;
② 。