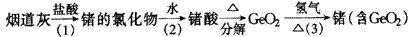1.下列物质的晶体中,不存在分子的是(??)。?
A.二氧化硅
B.二氧化硫
C.二氧化碳
D.二氧化氯
2.某二价金属碳酸盐和碳酸氢盐的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为6∶5,该混合物中碳酸盐和碳酸氢盐的物质的量之比为(??)。?
A.1∶1
B.1∶2
C.1∶3
D.1∶4
3.某无色混合气体可能含有CO2、CO、H2O(g)、H2中的一种或几种,依次进行如下连续处理(假定每步处理均反应完全):①通过碱石灰时,气体体积变小;②通过赤热的氧化铜时,固体变为红色;③通过白色硫酸铜粉末时,粉末变为蓝色;④通过澄清的石灰水时,溶液变得浑浊。由此可以确定原混合气体中(??)。?
A.一定含有CO2、H2O,至少含有H2、CO中的一种
B.一定含有H2O、CO,至少含有CO2、H2中的一种
C.一定含有CO、CO2,至少含有H2O、H2中的一种
D.一定含有CO、H2,至少含有H2O、CO2中的一种
4.高岭土的组成可表示为Al2Si2Ox(OH)y,其中x,y的数值分别是(??)。?
A.7,2
??B.5,4
??C.6,3
??D.3,6
5.某些保健品中含有锗(Ge)元素,它位于元素周期表的第四周期ⅥA族,有关锗的叙述正确的是(??)。?
A.二氧化锗具有强氧化性
B.锗的金属活动性比铝强
C.锗可以生成化学式为Na2GeO3的盐
D.锗是金属,可代替铜、铝制作电的导线
6.在SiO2+3C SiC+2CO的反应中,氧化剂与还原剂质量之比是(??)。
A.35∶60
??B.60∶36
??C.1∶2
??D.1∶3
7.根据碳族元素的相似性和递变性、一般性和特殊性的知识,判断下列说法中正确的是(??)。
A.CO2为弱氧化剂,而PbO2为强氧化剂
B.CO2和PbO2都是弱氧化剂,CO和PbO都是还原剂
C.Sn(OH)4可与NaOH反应,但不与盐酸反应
D.Ge单质的熔点介于Si、Pb之间,是半导体材料
8.如图1,已知:
SiC+2CO的反应中,氧化剂与还原剂质量之比是(??)。
A.35∶60
??B.60∶36
??C.1∶2
??D.1∶3
7.根据碳族元素的相似性和递变性、一般性和特殊性的知识,判断下列说法中正确的是(??)。
A.CO2为弱氧化剂,而PbO2为强氧化剂
B.CO2和PbO2都是弱氧化剂,CO和PbO都是还原剂
C.Sn(OH)4可与NaOH反应,但不与盐酸反应
D.Ge单质的熔点介于Si、Pb之间,是半导体材料
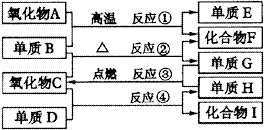
8.如图1,已知:
 |
|
图1 物质转化关系 |
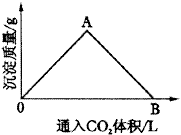
①单质E可作为半导体材料。 ②化合物F是不能生成盐的氧化物。 ③化合物I能溶于水呈酸性,它能够跟氧化物A起反应。 据此,请填空: (1)化合物F是___________。 (2)化合物I是___________。 (3)反应③的化学方程式___________。 (4)反应④的化学方程式___________。 9.在一定量饱和Ca(OH)2溶液中通入二氧化碳气体后,产生CaCO3白色沉淀的质量与二氧化碳体积之间的关系曲线如图2所示。试回答:
 |
|
图2 沉淀质量与CO2气体体积关系 |
(1)OA段曲线和AB段曲线所表示的反应方程式是:
OA___________;AB___________。
(2)A点时已参加反应的CO2和Ca(OH)2的物质的量之比为___________。
(3)B处溶液中存在浓度较大的两种离子是___________和___________(填离子符号)。将B处生成的溶液煮沸,可见到的现象是___________。
参考答案
第一节 1.A 2.D 3.C、D 4.B
5.(1)GeO2+4HCl GeCl4+2H2O
(2)GeCl4+3H2O
GeCl4+2H2O
(2)GeCl4+3H2O H2GeO3↓+4HCl
(3)GeO2+2H2
H2GeO3↓+4HCl
(3)GeO2+2H2 Ge+2H2O
第二节 1.C 2.D 3.B 4.(1)n=2,m=4 (2)119?
5.(1)Na2O·3FeO·Fe2O3·8SiO2·H2O
(2)Mg2Si2O8·nH2O+4HCl=2MgCl2+3SiO2+(n+2)H2O
(3)8 2KAlSi3O8--→K2O·Al2O3·6SiO2
第三节 1.A 2.B、D 3.D 4.(1)A、C、D
Ge+2H2O
第二节 1.C 2.D 3.B 4.(1)n=2,m=4 (2)119?
5.(1)Na2O·3FeO·Fe2O3·8SiO2·H2O
(2)Mg2Si2O8·nH2O+4HCl=2MgCl2+3SiO2+(n+2)H2O
(3)8 2KAlSi3O8--→K2O·Al2O3·6SiO2
第三节 1.A 2.B、D 3.D 4.(1)A、C、D
|
(2) |
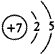 Si3N4 Si3N4 |
(3)Si3N4+12HF 3SiF4+4NH3
(4)3SiCl4+2N2+6H2
3SiF4+4NH3
(4)3SiCl4+2N2+6H2 Si3N4+12HCl
全章训练 1.A 2.B 3.D 4.B 5.C 6.C 7.A、D 8.(1)CO (2)HF (3)2H2+O2
Si3N4+12HCl
全章训练 1.A 2.B 3.D 4.B 5.C 6.C 7.A、D 8.(1)CO (2)HF (3)2H2+O2 2H2O
(4)2F2+2H2O
2H2O
(4)2F2+2H2O 4HF+O2↑
9.(1)Ca(OH)2+CO2
4HF+O2↑
9.(1)Ca(OH)2+CO2 CaCO3↓+H2O
CaCO3+CO2+H2O
CaCO3↓+H2O
CaCO3+CO2+H2O Ca(HCO3)2
(2)1∶1 (3)Ca2+和HCO3- 生成白色沉淀
Ca(HCO3)2
(2)1∶1 (3)Ca2+和HCO3- 生成白色沉淀