2. [四川省乐山市2009届高三上学期第一次调研考试]
|
|
元素代号 |
U |
V |
W |
X |
Y |
Z |
.M |
|
原子半径/nm |
0.037 |
0.157 |
0.074 |
0.075 |
0.077 |
0.143 |
0.102 |
|
主要化合价 |
+1 |
+1 |
-2 |
-3,+5 |
+2,+4 |
+3 |
-2,+6 |
请回答:
(1)X在元素周期表中的位置是 ;
(2)V、W、Z三种元素的离子具有相同的电子层结构,三者的离子半径由大到小顺是
(用元素符号表示);并用离子方程式表示出Z离子可作净水剂的
原因 。
(3)M的单质能跟V的最高价氧化物水化物的热浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式____________ _____ _。
(4)W、X、Y分别与U均可形成10电子共价化合物,晶体类型均为 ,其中,属于非极性分子的是(写化学式)__ ,若将其作为燃料,以熔融的K2CO3为电解质,空气作为氧化剂,并选择适当的隋性电极,组成原电池。写出该电池工作时的负极反应式 。
答案.(1)第二周期VA族(2分);
(2)O2-> Na+ > Al3+ (2分), Al
3++3H2O 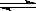 Al(OH)3(胶体)+3H+(2分);
Al(OH)3(胶体)+3H+(2分);
(3)3S+6OH-=2S2-+SO32-+3H2O(3分);
(4)分子晶体(2分)、CH4(2分)、CH4+4CO32--8e-=5CO2+2H2O (3分)。
25、(9分)向含a mol FeI2和b mol FeBr2的混合液中逐渐通入c mol Cl2,试分别填写不同c值范围内被氧化的离子及其物质的量。
|
c值范围 |
被氧化的离子符号 |
被氧化离子的物质的量/mol |
|
0<c≤a |
① |
② |
|
a<c≤(3a+b)/2 |
③ |
④ |
|
(3a+b)/2<c≤3(a+b)/2 |
⑤ |
⑥ |
答案.①I- ②2c ③Fe2+ ④2c-2a ⑤Br- ⑥2c-3a-b
 WXY2+W2Y, 得出上面结论的理由是:
WXY2+W2Y, 得出上面结论的理由是: 答案..(15分)(1)三周期ⅠA族 (2分)
答案..(15分)(1)三周期ⅠA族 (2分)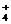 + H2O
+ H2O NH3·H2O+H
NH3·H2O+H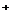 (2分)
(2分)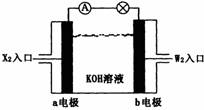 (1)Z2的电子式为
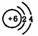
,Y的原子结构示意图为
,YW2的结构式为
。
(1)Z2的电子式为
,Y的原子结构示意图为
,YW2的结构式为
。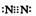
 O=C=O
(各2分)
O=C=O
(各2分) NH3↑+2H2O+ CO32-
(3分)
NH3↑+2H2O+ CO32-
(3分)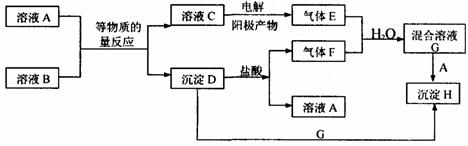 (鞍山市13中学2009届高三第三次模拟考试)
(10分)A、B均为无色盐溶液,B的焰色反应呈黄色,一定条件下A、B可以发生图所示的物质之间的一系列变化:
(鞍山市13中学2009届高三第三次模拟考试)
(10分)A、B均为无色盐溶液,B的焰色反应呈黄色,一定条件下A、B可以发生图所示的物质之间的一系列变化: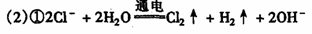 (2分)
(2分)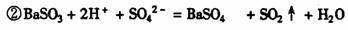 (2分)
(2分) 学)氟气是氧化性最强的非金属单质。等物质的量的F2与NaOH在稀溶液中反应生成NaF、H2O和一种气体,该气体是( B )
学)氟气是氧化性最强的非金属单质。等物质的量的F2与NaOH在稀溶液中反应生成NaF、H2O和一种气体,该气体是( B )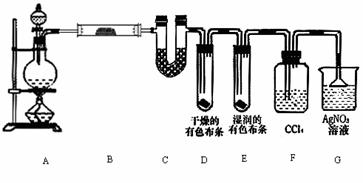 (16分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如右图所示的实验装置(支撑用的铁架台省略),按要求回答问题:
(16分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如右图所示的实验装置(支撑用的铁架台省略),按要求回答问题: MnCl2+C12↑+2H2O;
MnCl2+C12↑+2H2O;