6、下图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是
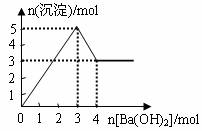
A.MgSO4 B.KAl(SO4)2 C.Al2(SO4)3 D.NaAlO2
19.(7分)设反应①Fe(s)+CO2(g)  FeO(s)+CO(g)的平衡常数为K1。
FeO(s)+CO(g)的平衡常数为K1。
反应②Fe(s)+H2O (g)  FeO(s)+H2 (g)的平衡常数为K2,在不同温度下K1、K2的值如下:
FeO(s)+H2 (g)的平衡常数为K2,在不同温度下K1、K2的值如下:
|
T(K) |
K1 |
K2 |
|
973 |
1.47 |
2.36 |
|
1173 |
2.15 |
1.67 |
(1)平衡常数K1的表达式为 。
(2)现有反应③CO2(g)+H2(g)  CO(g)+H2O(g),这是一个
(填“吸” 或“放”)热反应,要使反应③在一定条件下建立的平衡向右移动,可采取的措施的有
CO(g)+H2O(g),这是一个
(填“吸” 或“放”)热反应,要使反应③在一定条件下建立的平衡向右移动,可采取的措施的有
。
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
(3)若反应Fe(s)+CO2(g)
 CO(g)+H2O(g)
在温度T1下进行;
CO(g)+H2O(g)
在温度T1下进行;
Fe(s)+H2O(g)  FeO(s)+H2 (g)在温度T2下进行,已知T1>T2,且c(CO2)>c(H2O)(其他条件均相同),则两者的反应速率
(填序号)
FeO(s)+H2 (g)在温度T2下进行,已知T1>T2,且c(CO2)>c(H2O)(其他条件均相同),则两者的反应速率
(填序号)
A.前者大 B.后者大 C.一样大 D.无法判断
17.(12分)现有下列短周期元素性质的数据:
 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径(10-10m) |
0.73 |
1.02 |
1.34 |
1.06 |
0.99 |
1.54 |
0.75 |
1.18 |
|
最高或最低化合价 |
|
+6 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
-2 |
|
-3 |
-1 |
|
-3 |
|
试回答下列问题:
(1)元素③在周期表中的位置是 ;元素④与元素⑦相比较,气态氰化物较稳定 的是 (填化学式);
(2)元素①与元素⑥按照原子个数比为1:1形成的化合物中化学键的类型为
。
(3)Y和Z均由元素①组成,反应Y+2I-+2H+===I2+Z+H2O常作为Y的鉴定反应。
Ⅰ.Y与Z的关系是(选填字母) :
a.同位素 b.同素异形体 c.同系物 d.同分异构体
Ⅱ.将Y和二氧化硫分别通入品红溶液,都能使品红褪色。简述用褪色的溶液区分二者的实验方法 ;
(4)元素⑤的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式 ;
(5)元素①单质和元素⑧单质在海水中可以形成原电池,写出正极反应式:
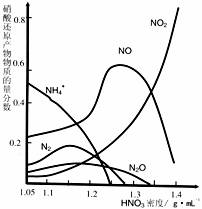
。18.(14分)金属(M)的腐蚀是因为发生反应:M-ne-→Mn+。金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大。一种钢铁防腐的方法是将钢铁放在冷的浓硝酸中浸泡。但是加热或在稀HNO3中,铁与 硝酸会不断反应。不同浓度的HNO3与铁反应的还原产物很复杂,其分布曲线如图。
(1)钢铁在冷的浓硝酸中浸泡能防腐的原因是:
。
(2)工业上一般不用冷浓硝酸进行铁表面处理,其可能的原因是:
。
(3)由图示可知,密度等于1.35 g·mL-1的硝酸与铁反应时,其还原产物主要是
;足量的铁与一定量的浓硝酸反应时,反应过程中可能的气体产物有 ;还原产物中NH4+的物质的量分数随 而增大;请用一句话概括该图反映出的基本结论: 。
(4)m mol 铁与极大量的密度为1.35 g·mL-1的硝酸溶液完全反应放出n L气体(体积 在标准状况下测定),此时溶液中Fe元素的存在方式是 , n 的值最接近 (填字母编号)。
A.22.4m B.33.6m C.44.8m D.67.2m
(5)除了上述处理的方法外,下列方法也能起到防腐作用的是 (填字母编号)
A.在铁中掺入铬、镍等金属,改变其内部结构,制成不锈钢
B.在铁制品表面镀锌
C.提高铁中含碳量,制成生铁
D.将水库铁闸门与直流电源的负极相连