18.(7分)几种短周期元素的原子半径及其某些化合价见下表:
|
元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
|
化合价 |
-1 |
-2 |
+4、-4 |
+4、-2 |
+5、-3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.102 |
0.110 |
0.143 |
0.160 |
0.186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题。涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中位于 周期, 族;
(2)A、H、J对应离子的半径由大到小的顺序是(填离子符号) ;
(3)A与J所形成化合物的晶体类型是 ,用电子式表示其形成过程
;
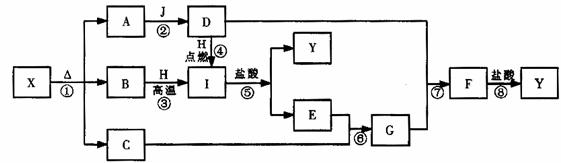
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为 ;D与B形成的某种化合物Y不仅能与X反应,还能与I的单质反应。则Y与I的单质反应的化学方程式为 。
15.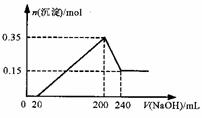 将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是 ( )
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是 ( )
A.Mg和Al的总质量为8g
|
C.生成的H2在标准状况下的体积为11.2L
D.NaOH溶液的物质的量浓度为5mol/L
第Ⅱ卷(非选择题,共55分)
13.下列实验不能达到预期目的的是 ( )
|
序号 |
实验内容 |
实验目的 |
|
A |
Cl2、Br2分别与H2反应 |
比较Cl2、Br2的非金属性强弱 |
|
B |
Cl2、S分别与Fe反应 |
比较Cl2、S的氧化性强弱 |
|
C |
测定相同浓度的Na2CO3、NaSO4两溶液的pH |
比较碳酸、硫酸的稳定性强弱 |
|
D |
测定相同浓度的盐酸、醋酸两溶液的导
电性 |
比较盐酸、醋酸的酸性强弱 |

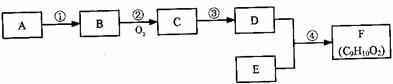
 请回答以下问题:
请回答以下问题: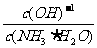 (填“增
(填“增