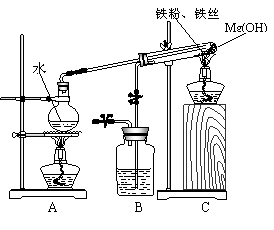
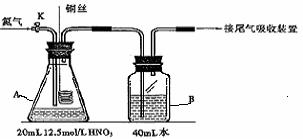
23、(6分)某化学活动小组为探究铜与硝酸反应还原产物主要为NO时硝酸的浓度,设计实验装置如下图所示(连接好仪器并检察气密性后,分别装入相对应的试剂):
Ⅰ.⑴实验开始时先打开活塞K持续通入N2一段时间后,关闭K。将铜丝(足量)下移伸入浓硝酸后,有大量的饿红棕色气体生成,随时间的进行,气体颜色逐渐变浅,当A中充满无色气体时:
①装置A中反应的离子方程式为 ;
②接下来的实验操作是 ;
⑵本实验中装置A的优点是 。
Ⅱ.将B中所得溶液稀释至200ml,用0.2mol/l的NaOH溶液进行中和滴定。实验数据如下(硝酸的挥发分解及溶液体积的变化忽略不计):
|
实验编号 |
待测液体积(ml) |
NaOH溶液体积(ml) |
|
1 |
20.00 |
15.98 |
|
2 |
20.00 |
14.99 |
|
3 |
20.00 |
 15.01 15.01 |
⑴待测液的浓度为 mol/l
⑵硝酸与铜反应主要生成NO时硝酸的浓度不大于 mol/l。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH-、C1-、CO32-、NO3-、SO42- |
22.(8分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(2)写出E溶液与过量的B溶液反应的离子方程式。 。
 (3)在100mL0.1mol·L-1E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀物质的量为
。
(3)在100mL0.1mol·L-1E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀物质的量为
。
 A.H2O + H2O H3O++
OH- B.CO32-+ H2O HCO3-+ OH-
A.H2O + H2O H3O++
OH- B.CO32-+ H2O HCO3-+ OH-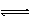
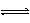 C.NH3 + H2O NH3·H2O
D.HCO3-+ H2O H3O++
CO32-
C.NH3 + H2O NH3·H2O
D.HCO3-+ H2O H3O++
CO32- TiO2、
TiO2、 TiO2、
TiO2、 TiO2互为同位素
TiO2互为同位素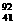 Nb3+原子核内有51个中子,核外有41个电子
Nb3+原子核内有51个中子,核外有41个电子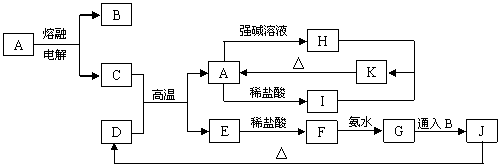 A~K是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已经略去)。已知A是一种高熔点的化合物,D是一种红棕色的固体,H的焰色反应呈黄色。
A~K是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已经略去)。已知A是一种高熔点的化合物,D是一种红棕色的固体,H的焰色反应呈黄色。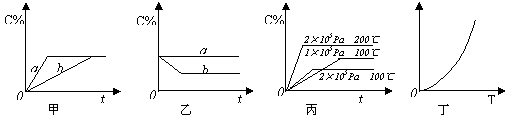 (8分)如下图,甲、乙、丙分别表示在不同条件下可逆反应:A(g)+B(g)
(8分)如下图,甲、乙、丙分别表示在不同条件下可逆反应:A(g)+B(g) xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
xC(g)的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。