在下列溶液中,各组离子一定能够大量共存的是( )
| A、在无色的溶液中:Na+、Cl-、SO42-、Fe3+ |
| B、使酚酞试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、常温下,水电离出的 c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、在pH=1的溶液中:NH4+、K+、ClO-、SO32- |
下列反应的离子方程式正确的是( )
A、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O
| ||||
B、电解饱和氯化铝溶液:2Cl-+2H2O
| ||||
C、实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-
| ||||
| D、向 NaHS 溶液中通入适量氯气:HS-+Cl2═S↓+H++2Cl- |
食用下列食品通常不会对人体健康造成危害的是( )
| A、用甲醛溶液浸泡的海鲜 |
| B、用工业食盐腌制的泡菜 |
| C、用工业酒精配制的白酒 |
| D、牛奶经发酵后得到的酸奶 |
 镁_次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主 要工作原理如右图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )
镁_次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主 要工作原理如右图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )| A、该电池中镁为负极,发生还原反应 |
| B、电池工作时,OH-向正极移动 |
| C、电池工作时,正极周围溶液的pH将不断变小 |
| D、该电池的总反应式为:Mg+ClO-+H2O═Mg(OH)2↓+Cl- |
2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的主要反应之一.一定温度下,在甲、乙、丙、丁四个容器体积均为2L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
下列判断中,正确的是( )
| 甲 | 乙 | 丙 | 丁 | ||
| 起始物质的量 | n(SO2)/mol | 0.40 | 0 | 0.80 | 0.02 |
| n(O2)/mol | 0.24 | 0 | 0.48 | 0.04 | |
| n(SO3)/mol | 0 | 0.40 | 0 | 0.40 | |
| 含硫反应物的平衡转化率% | 80 | α1 | α2 | α3 | |
| A、乙中SO3的平衡转化率为α1=20% |
| B、平衡时,丙中c(SO3)是甲中的2倍 |
| C、平衡时,α3<α1 |
| D、该温度下,平衡常数的值为400 |
金属铜与人体分泌物中的盐酸以及子宫内的空气反应可生成超氧酸:Cu+HCl+O2=CuCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是( )
| A、氧化剂是O2 |
| B、HO2在碱中能稳定存在 |
| C、氧化产物是HO2 |
| D、1molCu参加反应有2mol电子发生转移 |
下列各组物质中,互为同系物的是( )
A、CH3-CH=CH2和 |
B、 和 和 |
C、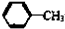 和 和 |
| D、CH2=CH-CH=CH2和CH3-CH2-CH2-C≡CH |
下列关于乙醇的说法中,正确的是( )
| A、分子中含有C=O键 |
| B、官能团为羧基 |
| C、能使紫色石蕊试液变红 |
| D、可用碳酸钠溶液来鉴别乙醇和乙酸溶液 |
Na2O2、Cl2、SO2等均能使品红溶液褪色.下列说法正确的是( )
| A、Na2O2、Cl2、SO2依次属于电解质、非电解质、非电解质 |
| B、标准状况下,1mol Na2O2和22.4LSO2反应生成Na2SO4,转移电子1mol |
| C、等物质的量Cl2和SO2同时通入品红溶液,褪色更快 |
| D、在Na2O2中阴阳离子所含的电子数目不相等 |
将5.6g铁粉投入足量的100mL 2mol/L稀硫酸中,2min时铁粉刚好完全溶解.下列有关这个反应的反应速率表示不正确的是( )
| A、铁的反应速率=0.5mol/(L?min) |
| B、硫酸的反应速率=0.5mol/(L?min) |
| C、硫酸亚铁的反应速率=0.5mol/(L?min) |
| D、氢气的反应速率=0.5mol/(L?min) |