题目内容
在下列溶液中,各组离子一定能够大量共存的是( )
| A、在无色的溶液中:Na+、Cl-、SO42-、Fe3+ |
| B、使酚酞试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、常温下,水电离出的 c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、在pH=1的溶液中:NH4+、K+、ClO-、SO32- |
考点:离子共存问题
专题:离子反应专题
分析:A.Fe3+为黄色;
B.使酚酞试液变红的溶液,显碱性;
C.常温下,水电离出的 c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液;
D.pH=1的溶液,显酸性,离子之间发生氧化还原反应.
B.使酚酞试液变红的溶液,显碱性;
C.常温下,水电离出的 c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液;
D.pH=1的溶液,显酸性,离子之间发生氧化还原反应.
解答:
解:A.Fe3+为黄色,与无色溶液不符,故A错误;
B.使酚酞试液变红的溶液,显碱性,碱性溶液中不能大量存在Fe2+、Mg2+,故B错误;
C.常温下,水电离出的 c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液,酸、碱溶液中该组离子之间均不反应,可大量共存,故C正确;
D.pH=1的溶液,显酸性,H+、ClO-、SO32-离子之间发生氧化还原反应,不能大量共存,故D错误;
故选C.
B.使酚酞试液变红的溶液,显碱性,碱性溶液中不能大量存在Fe2+、Mg2+,故B错误;
C.常温下,水电离出的 c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液,酸、碱溶液中该组离子之间均不反应,可大量共存,故C正确;
D.pH=1的溶液,显酸性,H+、ClO-、SO32-离子之间发生氧化还原反应,不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
居里夫人因发现了镭元素获得1911年诺贝尔化学奖,距今百年,这也是居里夫人第二次获得诺贝尔奖,广为世人称道.下列关于镭的性质的描述中不正确的是( )
| A、在化合物中呈+2价 |
| B、氢氧化物呈两性 |
| C、单质与水反应,放出氢气 |
| D、碳酸盐难溶于水 |
国际上已禁止民用产品使用石棉制品,避免吸入石棉纤维而诱发肺病.某种石棉的化学式可表示为:Ca2MgxSiyO22(OH)2,式中x、y的值分别为( )
| A、8,3 | B、5,8 |
| C、3,8 | D、8,5 |
已知某离子的结构示意图如图 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、该元素位于第二周期第ⅡA族 |
| B、该元素位于第二周期第Ⅷ族 |
| C、该元素位于第三周期第ⅡA族 |
| D、该元素位于第三周期0族 |
金属铜与人体分泌物中的盐酸以及子宫内的空气反应可生成超氧酸:Cu+HCl+O2=CuCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是( )
| A、氧化剂是O2 |
| B、HO2在碱中能稳定存在 |
| C、氧化产物是HO2 |
| D、1molCu参加反应有2mol电子发生转移 |
已知下述三个实验均能发生化学反应.下列判断正确的是( )
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铜丝放入氯化铁溶液中 |
| A、上述实验证明氧化性:Fe3+>Fe2+>Cu2+ |
| B、实验①中铁钉只作还原剂 |
| C、实验②中Fe2+既显氧化性又显还原性 |
| D、实验③中发生的是置换反应 |
化学平衡状态是( )
| A、静止止状态 |
| B、正反应速率大于逆反应速率 |
| C、不可改变的状态 |
| D、反应物与生成物浓度保持不变的状态 |
下列实验方法或操作正确的是( )
A、 转移溶液 |
B、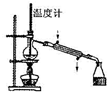 制蒸馏水 |
C、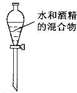 分离水合酒精 |
D、 稀释浓硫酸 |
不能用排水收集法收集的气体是( )
| A、氨气 | B、氧气 |
| C、二氧化硫 | D、一氧化氮 |