题目内容
 镁_次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主 要工作原理如右图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )
镁_次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主 要工作原理如右图所示,其正极反应为:ClO-+H2O+2e-═Cl-+2OH-,关于该电池的叙述正确的是( )| A、该电池中镁为负极,发生还原反应 |
| B、电池工作时,OH-向正极移动 |
| C、电池工作时,正极周围溶液的pH将不断变小 |
| D、该电池的总反应式为:Mg+ClO-+H2O═Mg(OH)2↓+Cl- |
考点:原电池和电解池的工作原理
专题:有机物的化学性质及推断
分析:该原电池中,镁作负极,负极上镁失电子发生氧化反应,正极上次氯酸根离子得电子发生还原反应,电池反应式为:Mg+ClO-+H2O=Mg(OH)2↓+Cl-,原电池放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动.
解答:
解:A.负极发生氧化反应,故A错误;
B.原电池原理中,阴离子向负极移动,阳离子向正极移动,故B错误;
C.正极反应为ClO-+H2O+2e-═Cl-+2OH-,电池工作时,在正极附近生成OH-,故pH增大,故C错误;
D.负极上镁失电子,正极上次氯酸根离子得电子,所以电池反应为Mg+ClO-+H2O=Mg(OH)2↓+Cl-,故D正确;
故选D.
B.原电池原理中,阴离子向负极移动,阳离子向正极移动,故B错误;
C.正极反应为ClO-+H2O+2e-═Cl-+2OH-,电池工作时,在正极附近生成OH-,故pH增大,故C错误;
D.负极上镁失电子,正极上次氯酸根离子得电子,所以电池反应为Mg+ClO-+H2O=Mg(OH)2↓+Cl-,故D正确;
故选D.
点评:本题考查原电池(燃料电池)基本原理,为高频考点,侧重于学生的分析能力的考查,本题涉及电极判断、电极反应书写、离子流动等相关知识,难度不大.

练习册系列答案
相关题目
下列各物质中,能形成顺反异构体的是( )
| A、1-丁烯 |
| B、丙烯 |
| C、2-甲基-2-丁烯 |
| D、2,3-二氯-2-丁烯 |
下列四组等质量的铁与过量的盐酸在不同条件下反应,反应速率由快到慢的顺序排列正确的是( )
| 组别 | c(HCl/mol/L) | 温度/℃ | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 粉末状 |
| 4 | 2.5 | 30 | 粉末状 |
| A、4-3-2-1 |
| B、1-2-3-4 |
| C、3-4-2-1 |
| D、1-2-4-3 |
下列物质不属于醛类的是( )
A、 |
B、 |
| C、CH2═CH-CHO |
| D、CH3-CH2-CHO |
Na2O2、Cl2、SO2等均能使品红溶液褪色.下列说法正确的是( )
| A、Na2O2、Cl2、SO2依次属于电解质、非电解质、非电解质 |
| B、标准状况下,1mol Na2O2和22.4LSO2反应生成Na2SO4,转移电子1mol |
| C、等物质的量Cl2和SO2同时通入品红溶液,褪色更快 |
| D、在Na2O2中阴阳离子所含的电子数目不相等 |
下列说法中错误的是( )
| A、化学反应并不一定伴随发生能量变化 |
| B、煤、石油、天然气是目前世界最重要的能源 |
| C、我国农村建沼气池所生产的沼气是一种清洁能源 |
| D、人体运动所消耗的能量与化学反应有关 |
下列分子的空间构型为三角锥形的是( )
| A、CO2 |
| B、NH3 |
| C、CO2 |
| D、BF3 |
在硫酸钠和硫酸钾的混和溶液中,当n(Na+)=0.2mol,n(SO42-)=x mol,n(K+)=y mol时,则x和y的关系是( )
| A、y=2(x+0.1) | ||
B、x=
| ||
| C、y=2x-0.1 | ||
D、x=0.1+
|
下列有机物的系统命名正确的是( )
A、 异丁烷 |
B、 2-甲基-3-丁烯 |
C、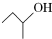 2-丁醇 |
D、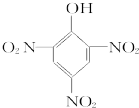 1,3,5-三硝基苯酚 |