11.原子序数递增的部分短周期主族元素的原子半径数据如下表:
|
元素 |
A |
B |
D |
E |
F |
G |
M |
N |
P |
|
原子半径/nm |
0.077 |
0.075 |
0.074 |
0.071 |
0.186 |
0.160 |
0.143 |
0.102 |
0.099 |
(1)已知[A、B、D、E、N、P为非金属元素,且均不与F、G、M中任何一种元素同族,在周期表中的相对位置如下,请将相应元素符号填在表中。
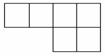
(2)B在周期表中的位置为____________,AD2的电子式为____________。(3)N的最高价氧化物的水化物与A单质反应的化学方程式为____________ 。(4)M的最高价氧化物的水化物是药物“胃舒平”的主要成分,可以治疗胃酸过多,反应的离子方程式为
-______________________________________________________ ,F的最高价氧化物的水化物也可以中和胃
酸,不用其治疗胃酸过多的原因是____________ 。
(5)AD2与ND2性质相似,G在ND2中也可以剧烈燃烧,可能的产物是____________,反应的化学方程式为-____________________________________。
9.下表是元素周期表的一部分,已知元素⑤⑥⑦均可构成电子数为18的微粒。
|
① |
② |
③ |
④ |
|
|
|
|
⑤ |
⑥ |
⑦ |
(1)某元素能形成的化合物种类最多,该元素是____________(填编号)。该元素有多种同位素,在科学上均有重要的应用,写出其中任意一种同位素的某一项用途-______________________________________________________ 。
(2)⑤号元素可形成两种18电子的阴离子,其离子符号分别为____________、____________。
(3)①~⑥号六种元素的简单氢化物中,沸点最高的是-__________________ (填分子式)。
(4)①~⑦号七种元素中,原子半径最小的元素具有的性质是____________(填序号)。
A.单质可与水反应,形成两种化合物
B.单质可与⑥的钠盐溶液反应,置换出元素⑥的单质
C.气态氢化物的水溶液呈弱酸性
D.可以用玻璃器皿在实验室制取该元素的气态氢化物
8.从下列事实所得出的相应结论正确的是( )
|
|
实验事实 |
结论 |
|
A |
A元素的原子半径比B元素的原子半径大 |
周期表中A位于B的下一周期 |
|
B |
将CO2通入到Na2SiO3溶液中产生白色浑浊(H2SiO3) |
酸性:H2CO3>H2SiO3 |
|
C |
将燃烧的镁条放入CO2中能继续燃烧 |
还原性:Mg>C |
|
D |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
7.(2009年潍坊模拟)现有下列短周期元素的数据
 元素编号元素性质 元素编号元素性质 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径 |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
0.82 |
|
最高化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
最低化合价 |
-2 |
|
|
-3 |
-1 |
|
-3 |
|
下列说法中,正确的是( )
A.元素原子序数④小于⑦
B.②、③号元素处于同一周期
C.⑤号元素最高价氧化物的水化物酸性最强
D.⑧号元素是非金属元素

