8.(15分)
(1)蒸馏法(1分)、离子交换法(其它答案合理给分)(1分)
(2)Cl2(1分)、NaOH(1分)、NaClO(1分)
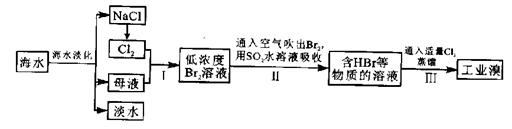
(3)富集溴元素(1分)
(4)Br2+SO2+2H2O=4H++SO42-+2Br-(2分),强酸对设备的严重腐蚀(1分)
(5)①冷凝管(1分) ②Br2腐蚀橡胶(1分)
③控制温度计b的温度,并收集59℃是的馏分(2分)
④深红棕色(1分),分液(或蒸馏)(1分)
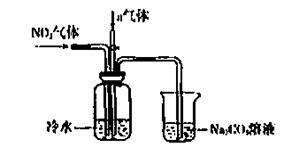 9/某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)
9/某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)
(1)工业上用氨气制取NO的化学方程式是 。
(2)连接好装置后,首先进行的操作是 。
(3)通入a气体的目的是 .
(4)盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中发生反应的化学方程式是
2NO2+Na2CO3=====NaNO2+ +
(5)已知:温度低于21.15°C时,NO2几乎全部转变为N2O2。工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是 。
 (6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=
。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为
。
(6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=
。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为
。
|
|
 =====4NO+6H2O
=====4NO+6H2O
(2)检验装置的气密性
(3)提高NO2的转化率(或2NO+O2=2NO2)(合理均给分)
(4)NaNO3 CO2
(5)2N2O4+O2+2H2O=4HNO3[来源:高&考%资(源#网]
(6)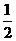 50%
50%
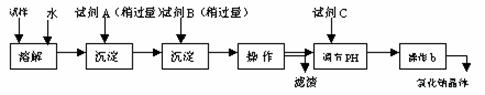
5.(10分)工业上以锂辉石(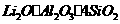 ,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
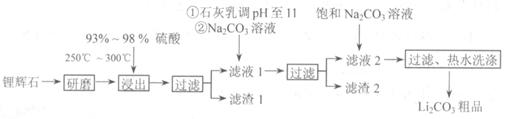
已知:①
②某些物质的溶解度(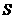 )如下表所示。
)如下表所示。
|
T/℃ |
20 |
40 |
60 |
80 |
|
S(Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
|
S(Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
(1)从滤渣1中分离出A12O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤II中反应的离子方程式是 。
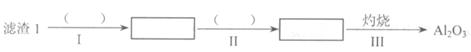
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡原理简述) 。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是 。
②b中,生成Li2CO3反应的化学方程式是 。
4.(12分)某化学兴趣小组以碳和浓硝酸为起始原料,想利用一氯化氮与过氧化钠反应制备亚硝酸钠。设计装置如下:(忽略装置中空气的影响)
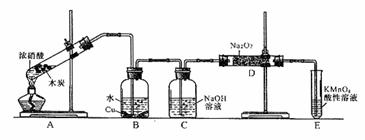
请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是 。
(2)猜测B中可以观察的主要现象是
。C瓶出来的气体是 。
(3)已知:①室温下存在反应3HNO2=HNO3+2NO↑+H2;②在酸性溶液中,NO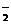 可将MnO
可将MnO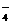 还原为Mn2+且无气体生成。写出检验D中产物是亚硝酸钠的方法:
还原为Mn2+且无气体生成。写出检验D中产物是亚硝酸钠的方法:
。
(4)E装置的作用是 。
(5)同学们经过讨论认为上述装置仍有缺陷,为避免D管中生成NaOH,你认为应该进行的改进是 。
|
(1)C+4HNO3(浓) CO2↑+4NO2↑+2H2O
(2)溶液逐渐变蓝;NO(或一氧化氮);
(3)方法I:将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠。反应的离子方程式是3NO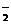 +2H+=NO
+2H+=NO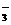 +2NO↑+H2O
+2NO↑+H2O
方法II:将生成物置于试管中,加入酸性KMnO4溶液,若溶液紫色褪去,则D中产物是亚硝酸钠,反应的离方程式是5 NO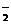 +2MnO
+2MnO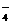 +6H+=5
NO
+6H+=5
NO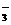 +2Mn2++3H2o
+2Mn2++3H2o
(其它合理答案均得分)
(4)吸收D中未反应完的NO,以免污染空气(其它合理答案均得分)
(5)在C、D之间增加一个盛浓硫酸的洗气瓶(或装无水CaCl2的干燥管)
(其它合理答案均得分)

 [来源:
[来源: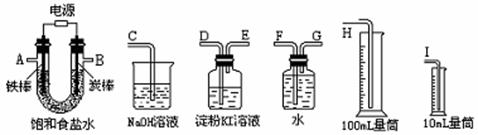
 HClO+OH-
HClO+OH-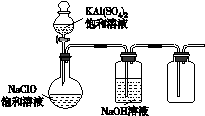 (4)某小组同学用右图所示装置探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。
(4)某小组同学用右图所示装置探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。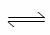 (1)(2分)Al3++3NH3·H2O=Al(OH)3 ↓+3NH4+
(1)(2分)Al3++3NH3·H2O=Al(OH)3 ↓+3NH4+ Mg2+
Mg2+ (2)NH
(2)NH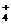 +H2O NH3·H2KO+H+
+H2O NH3·H2KO+H+