15. 现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
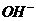 、 、 、 、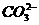 、 、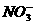 、 、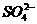 |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)分别写出A、B、C、D、E的化学式:A 、B 、C 、
D 、E ;
(2)写出A、E反应的离子方程式: ;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H =-Q kJ·mol-1。
写出B与C稀溶液反应的热化学方程式 。
(5)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为 mol。
14. 复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下,测得浓度均为0.1mol/L的下列六种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
 复分解反应存在这样一个规律:一种较强酸与一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑
复分解反应存在这样一个规律:一种较强酸与一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑
若换个角度看,它同时还揭示出另一条规律,即碱性较强的物质发生类似反应可以
生成碱性较弱的物质。依照该规律,请你判断下列反应不能成立的是 (填编号)
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.CH3COOH+NaCN=CH3COONa+HCN
(2)根据前述信息判断,浓度均为0.05mol/L的下列六种物质的溶液中,pH最小的是
(填编号),其pH为 (填数值);pH最大的是 (填编号);
①HClO4 ②CH3COOH ③HCN ④HClO ⑤H2SO4
(3)一些复分解反应的发生还遵循其他的规律。下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②工业上将石灰乳与苦卤(主要溶质KCl、MgCl2)混合可得氢氧化镁固体
③蒸馏KCl和NaNO3混合溶液,首先析出NaCl晶体
请根据上述反应,总结出复分解反应发生的另一个规律:
。
将KI溶液与AgCl固体混合搅拌,固体变为黄色。该反应也遵循这一规律,请写出反应的化学方程式: 。
II.设计出燃料电池使汽油氧化直接产生电流是对21世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。回答如下问题:
 (1)以庚烷(C7H16)代表汽油,这个电池放电时发生的化学反应的化学方程式是:
(1)以庚烷(C7H16)代表汽油,这个电池放电时发生的化学反应的化学方程式是:
(2)这个电池的负极发生的反应是:C7H16+22O2--44e-=7CO2+8H2O
正极发生的反应是:
固体电解质里的O2-向 极移动
(3)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:
(4)汽油燃料电池最大的障碍是氧化反应不完全产生 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,正是新一代化学家的历史使命。
 可将B2-氧化为B单质,A2O
可将B2-氧化为B单质,A2O H2CO3
B.2Na2O2+2H2O=4NaOH+O2↑
H2CO3
B.2Na2O2+2H2O=4NaOH+O2↑ Fe2O4+4H2
D.2Na+2H2O=2NaOH+H2↑
Fe2O4+4H2
D.2Na+2H2O=2NaOH+H2↑ H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是
kJ
H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是
kJ N2H4+H3O+=N2H5++H2O N2H4+H2O N2H5++
N2H4+H3O+=N2H5++H2O N2H4+H2O N2H5++ 2SO3(g);△H=-197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO2、1molO2
和1molSO3、1molSO2、0.5mol
O2,当它们分别达到平衡时放出的热量为Q1 KJ和Q2KJ,则下列比较正确的是( )
2SO3(g);△H=-197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO2、1molO2
和1molSO3、1molSO2、0.5mol
O2,当它们分别达到平衡时放出的热量为Q1 KJ和Q2KJ,则下列比较正确的是( )
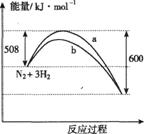 右图是198K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是( )
右图是198K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是( ) 2NH3
△H=-92kJ·mol-1
2NH3
△H=-92kJ·mol-1