15. 短周期主族元素A、B、C、D、E的原子序数依次增大,它们的原子核外电子层数之和为10;B的化合物种类繁多,数目庞大。C、D是空气中含量最多的两种元素;D、E两单质可以生成两种不同的离子化合物
短周期主族元素A、B、C、D、E的原子序数依次增大,它们的原子核外电子层数之和为10;B的化合物种类繁多,数目庞大。C、D是空气中含量最多的两种元素;D、E两单质可以生成两种不同的离子化合物
(1)写出E的单质与A、D两元素形成其常见化合物反应的离子方程式________________________。
(2)由A、C、D三元素所形成的常见盐与氢氧化钠反应的方程式为_________________
(3)B的相对分子质量最小的氢化物,写出其化学式___________。
(4)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,某温度下相互转化时的量变关系如下图:
|
|

(I)X的化学式是___________
(II)图中a、b、c、d四点中,表示反应处于平衡状态的是___________
(III)反应进行到t2时刻,改变的条件可能是___________
[答案](1)2Na+2H2O=2Na++OH-+H2↑ (2分)(2)NH4NO3+NaOH=NaNO3+ NH3·H2O (2分)
(3)CH4(1分)(4)(I)NO2(1分)(II)b(1分)(III)增大NO2的浓度(合理)(1分)
 [解析]先推测这5种元素,B的化合物种类繁多,数目庞大,B为碳元素,C、D是空气中含量最多的两种元素,所以C是氮元素,D是氧元素,D、E两单质可以生成两种不同的离子化合物,则E是钠元素,生成的两化合物为Na2O、Na2O2,根据五种元素的原子核外电子层数之和为10,得到A元素是H,(1)即为钠和水的反应:2Na+2H2O=2Na++OH-+H2↑;(2)A、C、D三元素所形成的常见盐为NH4NO3;(3)B的相对分子质量最小的氢化物是CH4(4)(I)由题意可知,两种氮的氧化物价态相同,则为NO2、N2O4.根据t1时刻的数据,△C(Y)=0.2mol·L-1,△C(X)=0.4mol·L-1,由反应:N2O4
[解析]先推测这5种元素,B的化合物种类繁多,数目庞大,B为碳元素,C、D是空气中含量最多的两种元素,所以C是氮元素,D是氧元素,D、E两单质可以生成两种不同的离子化合物,则E是钠元素,生成的两化合物为Na2O、Na2O2,根据五种元素的原子核外电子层数之和为10,得到A元素是H,(1)即为钠和水的反应:2Na+2H2O=2Na++OH-+H2↑;(2)A、C、D三元素所形成的常见盐为NH4NO3;(3)B的相对分子质量最小的氢化物是CH4(4)(I)由题意可知,两种氮的氧化物价态相同,则为NO2、N2O4.根据t1时刻的数据,△C(Y)=0.2mol·L-1,△C(X)=0.4mol·L-1,由反应:N2O4 2NO2,物质的量浓度的变化之比等于计量数之比,所以X是NO2,Y是N2O4(II)a、b、c、d四点中,b点时,两物质的浓度都没有变化,在平衡状态;反应进行到t2时刻,NO2的浓度迅速增大,然后逐渐减小,N2O4的缓慢增大,平衡向着生成N2O4的方向移动。改变条件为增大NO2的浓度
2NO2,物质的量浓度的变化之比等于计量数之比,所以X是NO2,Y是N2O4(II)a、b、c、d四点中,b点时,两物质的浓度都没有变化,在平衡状态;反应进行到t2时刻,NO2的浓度迅速增大,然后逐渐减小,N2O4的缓慢增大,平衡向着生成N2O4的方向移动。改变条件为增大NO2的浓度
14.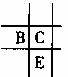 已知aA、bB、cC、dD、eE均为短周期元素,且原子序数依次增大。已知A、D同主族,A与其他元素均不同周期,B、C、E三种元素在周期表中的位置如图所示,且BC对应的单质在常温下为无色气体。请回答下列问题:
已知aA、bB、cC、dD、eE均为短周期元素,且原子序数依次增大。已知A、D同主族,A与其他元素均不同周期,B、C、E三种元素在周期表中的位置如图所示,且BC对应的单质在常温下为无色气体。请回答下列问题:
(1)A、B形成的四原子核化合物属于__________(填“极性”或“非极性”)分子,其易液化,原因是___________________________。
(2)由A、C两元素组成的三种10电子微粒是___________、____________、_______________
(3)甲是由A、C两元素形成的常见四原子核化合物,乙是由A、C、E形成的六原子核化合物,乙的水溶液和甲的水溶液相互反应的化学方程式为_____________________________。
(4)从五种元素中任选三种元素,组成化合物X和Y,在下列表格中按要求填写相应的化学式(每空只写一种即可)。
|
X
pH>7(25℃) |
Y
pH<7(25℃) |
|
抑制水的电离:____________________ |
抑制水的电离:____________________ |
|
促进水的电离:____________________ |
促进水的电离:____________________ |
[答案](1)极性;分子间存在氢键(2)H2O;OH-;H3O+(3)H2O2+H2SO3=H2SO4+H2O
(4)
|
X
pH>7(25℃) |
Y
pH<7(25℃) |
|
NaOH |
 H2SO4 H2SO4 |
|
NaHS |
NH4NO3 |
[解析]A与其他元素不同周期且原子序数最小,A为H,与之同主族元素D为Na,根据B、C、E在周期表中位置以及B、C的颜色状态,B为N,C为O,因此推断E为S。
所以A、B形成的四原子核化合物为NH3,极性分子,由于分子间存在氢键,沸点较高,容易液化。A、C组成的3种10电子微粒为H2O、OH-、H3O+。其中A和C组成的4原子核化合物为H2O2,具有氧化性,A、C、E形成的六原子核化合物具有还原性的为H2SO3,二者反应生成H2SO4。任选三种元素组成化合物,其中抑制水电离的为酸或者碱,如NaOH,H2SO4、HNO3等,促进水的电离的化合物为能水解的盐,如Na2SO3、NaHS、NH4NO3等。
13. 有关元素A、B、C、D、E的信息如下
有关元素A、B、C、D、E的信息如下
|
元素 |
有关信息 |
|
A |
元素主要化合价为-2,A的一种氢化物可用于实验室制取A的单质 |
|
B |
所在主族序数与所在周期序数之差为4 |
|
C |
原子中含10个P电子 |
|
D |
最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
|
E |
生活中常见金属,它有两种氯化物,相对原子质量相差35.5 |
请回答下列问题:
 (1)元素A-E中两种元素组成的化合物使品红溶液褪色的物质的化学式为_____________
(1)元素A-E中两种元素组成的化合物使品红溶液褪色的物质的化学式为_____________
(2)E元素与B元素可形成EB2和EB3两种化合物,下列说法正确的是(填序号)________。
①保存EB2溶液时,需向溶液中加入少量E单质
②EB2只能通过置换反应生成,EB3只能通过化合反应生成
③铜片、碳棒和EB3溶液组成原电池,电子由铜片沿导线流向碳棒
④向淀粉碘化钾溶液和苯酚溶液中分别滴加几滴EY3的浓溶液,原无色溶液都变为紫色
(3)用化学符号表示D2C的水溶液中各粒子的浓度关系,如c(C2-)=______________。
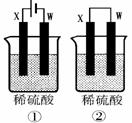
(4)将一定量的B单质通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中含有三种含B元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如下图所示。该苛性钾溶液中KOH的质量是___________,该反应中转移电子的物质的量是_________。
(5)工业上冶炼E单质的化学方程式为__________________________________
[答案](1)SO2、Na2O2
(2)①③
(3)c(S2-)= 1/2[c(Na+)+c(H+)- c(HS-)-c(OH-)]或c(S2-)= 1/2c(Na+)- c(HS-)-c(H2S)(其它合理答案也可)
(4)16.8g 0.21mol
(5)Fe2O3+3CO 3CO2+2Fe
3CO2+2Fe
 [解析]根据题给信息A为氧元素,实验室可以用双氧水来制备氧气;所在主族序数与所在周期序数之差为4,B元素为氧或者氯,因为A为氧,所以B为氯元素;C元素原子中含10个P电子,P电子一定为2p63p4,C元素为硫;最高价氧化物对应水化物,能电离出电子数相等的阴、阳离子,由于Mg(OH)2、Al(OH)3难溶,所以该物质为NaOH,D为钠元素;E有两种氯化物,相对原子质量相差35.5,E有变价,为Fe元素。
[解析]根据题给信息A为氧元素,实验室可以用双氧水来制备氧气;所在主族序数与所在周期序数之差为4,B元素为氧或者氯,因为A为氧,所以B为氯元素;C元素原子中含10个P电子,P电子一定为2p63p4,C元素为硫;最高价氧化物对应水化物,能电离出电子数相等的阴、阳离子,由于Mg(OH)2、Al(OH)3难溶,所以该物质为NaOH,D为钠元素;E有两种氯化物,相对原子质量相差35.5,E有变价,为Fe元素。
(1)漂白性物质包括化合漂白和氧化性漂白等,这几种元素中的两种元素形成的具有漂白性的物质有SO2、Na2O2
(2)FeCl2可以通过化合反应制得,如:2FeCl3+Fe=3FeCl2,FeCl3可以通过分解反应制得如2Fe(OH)3=Fe2O3+3H2O;淀粉碘化钾溶液中滴加几滴FeCl3的浓溶液,溶液呈蓝色,苯酚溶液中滴加几滴FeCl3的浓溶液,溶液显紫色,正确的说法为①③。
 (3)在Na2S溶液中,根据电荷守恒有:2c(S2-)+ c(HS-)+c(OH-)= c(Na+)+c(H+),根据物料守恒有:c(Na+)
= 2 [c(S2-)+c(HS-)+c(H2S)],变形即可。
(3)在Na2S溶液中,根据电荷守恒有:2c(S2-)+ c(HS-)+c(OH-)= c(Na+)+c(H+),根据物料守恒有:c(Na+)
= 2 [c(S2-)+c(HS-)+c(H2S)],变形即可。
(4)根据得失电子守恒,Cl2与KOH反应生成KClO、KClO3外,还有KCl生成,依据ClO-和ClO3-的物质的量配平方程式,有5Cl2+10KOH=7KCl+2KClO+KClO3+5H2O,转移电子0.03*7=0.21mol,反应消耗KOH的质量为0.03*10*56=16.8g。
(5)工业炼铁是用CO还原铁矿石制得
 (2分)取少量A于试管中,加入氢氧化钠溶液,加热,产生一种能够使湿润的红色石蕊试纸变蓝的气体,则证明阳离子是铵根离子。(2分)
(2分)取少量A于试管中,加入氢氧化钠溶液,加热,产生一种能够使湿润的红色石蕊试纸变蓝的气体,则证明阳离子是铵根离子。(2分) Fe3O4+4H2↑(2分)
Fe3O4+4H2↑(2分)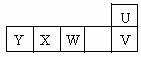 顺序依次排列,又因为U、W、Y最高价氧化物对应水化物之间能发生反应生成盐,所以W为铝,Y为钠,X在中间为镁。Z为血红蛋白中必需元素,Z为Fe。
顺序依次排列,又因为U、W、Y最高价氧化物对应水化物之间能发生反应生成盐,所以W为铝,Y为钠,X在中间为镁。Z为血红蛋白中必需元素,Z为Fe。 (2)
(2分)
(2)
(2分)
 D、A
D、A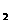 的电子式为______,B与D通常能形成______晶体,在E
的电子式为______,B与D通常能形成______晶体,在E
 分子 离子键、非极性键(或共价键)
分子 离子键、非极性键(或共价键)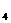 HCO
HCO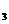 [或(NH
[或(NH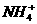 ,
,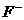 、
、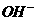 、NH2-;分子有:Ne、HF、H2O、NH3、CH4。根据题意知B溶于A后所得的物质可电离出阳离子C和阴离子D,可知A为H2O,B为NH3,氨气溶于水生成的一水合氨电离出
、NH2-;分子有:Ne、HF、H2O、NH3、CH4。根据题意知B溶于A后所得的物质可电离出阳离子C和阴离子D,可知A为H2O,B为NH3,氨气溶于水生成的一水合氨电离出