0 40947 40955 40961 40965 40971 40973 40977 40983 40985 40991 40997 41001 41003 41007 41013 41015 41021 41025 41027 41031 41033 41037 41039 41041 41042 41043 41045 41046 41047 41049 41051 41055 41057 41061 41063 41067 41073 41075 41081 41085 41087 41091 41097 41103 41105 41111 41115 41117 41123 41127 41133 41141 447348
 2H2O(l) △H= -142.9kJ·mol-1
2H2O(l) △H= -142.9kJ·mol-1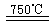 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg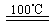 HgBr2+H2
HgBr2+H2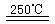 ______________ ④2HgO
______________ ④2HgO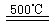 2Hg+O2↑
2Hg+O2↑
 CO2(g)+
H2(g); △H<0。在850℃时,K=1。
CO2(g)+
H2(g); △H<0。在850℃时,K=1。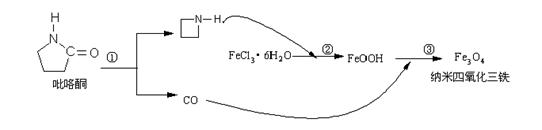
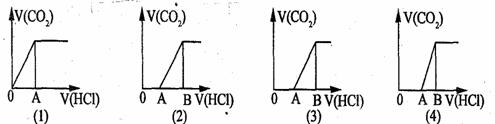
 3Y(g) +Z(g)。达到平衡时,有30%的X发生分解,则平衡时混合气体总物质的量是
3Y(g) +Z(g)。达到平衡时,有30%的X发生分解,则平衡时混合气体总物质的量是