17、(9分)A、B、M、X、Y、Z是周期表中的前20号元素,且原子序数依次增大。已知它们的部分化合物的性质如下:英才苑
|
A的最简氢化物 |
B的最简氢化物 |
M的最简氢化物 |
X的氧化物 |
Y的最简氢化物分子构型 |
Z的最高价氧化物 |
|
含氢量最高的有机物 |
水溶液呈碱性 |
水溶液呈酸性 |
两性氧化物 |
正四面体 |
对应的水化物为最强酸 |
回答下列问题:英才苑
(1)B的最简氢化物的分子构型是: 。英才苑
(2)M、X、Z三种元素的简单例子的离子半径由小到大的顺序是(用离子符号和“>”表示) 。英才苑
(3)已知M的单质与NaOH溶液反应的产物之一是OM2,试写出该反应的化学方程式:英才苑
。英才苑
(4)写出B的最简氢化物与Z的氢化物反应后生成物的电子式 。英才苑
(5)试比较A和Y的最高价氧化物熔点的高低(用“>”、“ <”或“=”表示); ,并说明理由 。英才苑
(6)A元素形成的氢化物有多种,1molA的某种氢化物分子中含有14mole-。已知在25℃,101kPa时1g该氢化物在足量氧气中充分燃烧生成液态水时放出的热量为50kJ,请写出该反应的热化学方程式: 。英才苑
14、有4组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如下表所示:英才苑
|
第一组 |
He -268.8 |
(a) -249.5 |
Ar -185.8 |
Kr -151.7 |
|
第二组 |
F2 -187.0 |
Cl2 -33.6 |
(b) 58.7 |
I2 184.0 |
|
第三组 |
(c) 19.4 |
HCl -84.0 |
HBr -67.0 |
HI -35.3 |
|
第四组 |
H2O 100.0 |
H2S -60.2 |
(d) 42.0 |
H2Te -1.8 |
下列各项判断正确的是英才苑
A、abc的化学式分别为Ne2、Br2、HF英才苑
B、第三组与第四组相比较,化合物的稳定顺序为:HBr>d英才苑
C、第三组物质溶于水后,溶液的酸性:c>HCl>HBr>HI英才苑
D、第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键英才苑
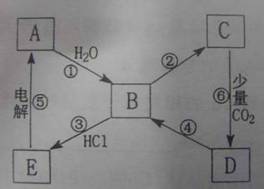 英才苑
英才苑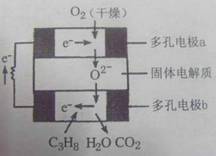 某固体燃料电池以固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是英才苑
某固体燃料电池以固体氧化铝--氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是英才苑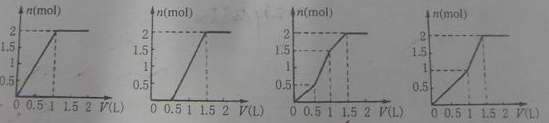 英才苑
英才苑