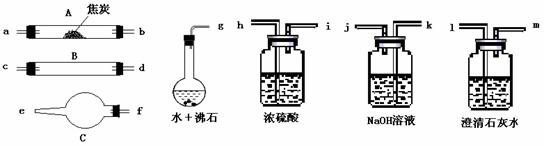
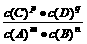22.(12分)某化学兴趣小组为探究铜跟浓硫酸的反应,用下图所示装置进行有关实验。
请回答下列有关问题:
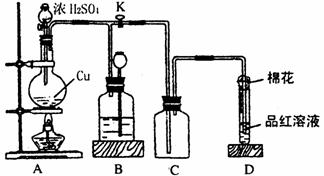
(1)装置A中发生的化学反应方程式为____________________________________________
(2)装置D中试管口放置的棉花中应浸一种液体,这种液体是_________________________,
其作用是______________________________________________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,
但由于余热的作用,A处仍有气体产生,此时B中现象是___________________________。
B中应放置的液体是(填字母)_____________。
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(4)实验中,取一定质量的铜片和一定体积18 mol · L – 1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是____________________________。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是________________(填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
 23.在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,
23.在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,
反应原理可用如下化学方程式表示:
NH3 + CO2 + NaCl + H2O == NH4Cl + NaHCO3↓
依据此原理,欲制得碳酸钠晶体,
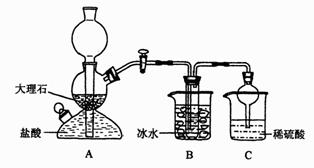
某校学生设计了如下实验装置,其中
B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
(1)A装置中所发生反应的离子方程式为: 。
C装置中稀硫酸的作用为: 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
|
|
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
|
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
|
NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
参照表中数据,请分析B装置中使用冰水是因为 。(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教
师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。现有下列试剂:盐酸、浓氨水、生石灰、蒸馏水,利用本题所提供的试剂(只限一种)及试管、酒精灯等主要仪器,通过简单实验判断该晶体是碳酸氢钠晶体,而不是碳酸氢铵或食盐晶体,简述操作方法、实验现象及结论:
。
 (5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为
。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为
。
18、下表中,对陈述I、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是
|
选项 |
陈述I |
陈述Ⅱ |
判断 |
|
A |
工业生产硫酸 用水吸收SO3 |
SO3可与水反应 |
I对;Ⅱ对;有 |
|
B |
Cl2和SO2混合后 可用于漂白纸浆 |
Cl2和SO2都有较好的漂白作用 |
I对;Ⅱ错;无 |
|
C |
金属钠具有强还原性 |
高压钠灯发出透雾性强的光 |
I对;Ⅱ对;无 |
|
D |
石墨常用作电解池的电极 |
石墨的化学性质稳定且导电性好 |
I对;Ⅱ对;有 |
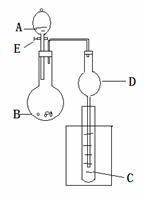
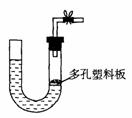 右图是气体制取装置,能用此装置制取气体并能“随开随用、随关随停”的是
右图是气体制取装置,能用此装置制取气体并能“随开随用、随关随停”的是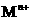 和
和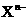 离子的物质的量浓度之间的关系近似于水的离子积
离子的物质的量浓度之间的关系近似于水的离子积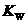 (
(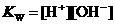 ,存在着
,存在着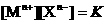 的关系(K为常数).现将足量的AgCl固体分别放入下列物质中,AgCl的溶解度由大到小排列的顺序是( )
的关系(K为常数).现将足量的AgCl固体分别放入下列物质中,AgCl的溶解度由大到小排列的顺序是( )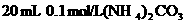 溶液 ②40 mL 0.03 mol/LHCl
溶液 ②40 mL 0.03 mol/LHCl 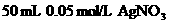 溶液 ④
溶液 ④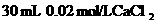 溶液
溶液  溶液
溶液 bB(g)
反应达平衡后,保持温度和压强不变,通入与反应混合物等物质的量的稀有气体,重新达到平衡时,B的浓度是原平衡时的60﹪。下列说法正确的是
( )
bB(g)
反应达平衡后,保持温度和压强不变,通入与反应混合物等物质的量的稀有气体,重新达到平衡时,B的浓度是原平衡时的60﹪。下列说法正确的是
( )  pC(g)+qD(g);△H<0。下列结论中正确的是
pC(g)+qD(g);△H<0。下列结论中正确的是