①称取2gCuSO4·5H2O研细后倒入烧杯,加10mL蒸馏水溶解
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤、晾干后研细备用。回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 ;
(2)步骤③中洗涤沉淀的操作是
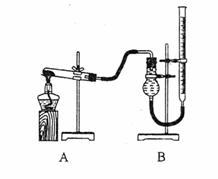 (二)证明氧化铜能加快氯酸钾的分角并与二氧化锰的催化效果进行比较用右图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
(二)证明氧化铜能加快氯酸钾的分角并与二氧化锰的催化效果进行比较用右图装置进行实验,实验时均以生成25mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KC1O3质量 |
其它物质质量 |
待测数据 |
|
④ |
1.2g |
无其他物质 |
|
|
⑤ |
1.2g |
CuO 0.5g |
|
|
⑥ |
1.2g |
MnO2 0.5g |
|
回答下列问题:
(3)上述实验中的“待测数据”指 ;
(4)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
(5)为探究CuO的实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a. ;
b.CuO的化学性质有没有改变。
12.(16分)已知物质A显酸性,F为七原子组成的环状物,请根据以下框图回答问题:
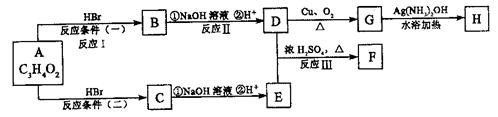
(1)写出下列物质的结构简式:A: ,
G: 。
(2)反应Ⅰ、Ⅱ、Ⅲ的反应类型分别为 、 、 。
(3)写出D和E反应生成F的化学方程式: 。
(4)写出C的同分异构体属于酯类物质的结构简式:(任写两种) 、 。
20.(8分)通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
键能/ KJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低Y(填>或<=SiC______ Si; SiCl4 ______ SiO2
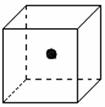 (2)右图立方体中心的“●”表示硅晶体中的一个原子,
(2)右图立方体中心的“●”表示硅晶体中的一个原子,
请在立方体的顶点用“●”表示出与之紧邻的硅原子。
(3)工业上高纯硅可通过下列反应制取:
 SiCl4 (g) + 2H2(g) Si(s) +
4HCl(g)
SiCl4 (g) + 2H2(g) Si(s) +
4HCl(g)
该反应的反应热△H = ___________ KJ/mol
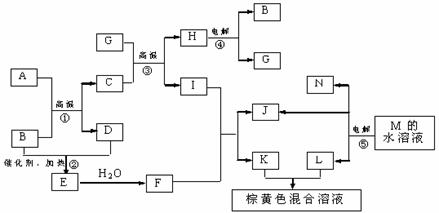 21.(8分)根据反应框图填空,已知反应①-⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120。
21.(8分)根据反应框图填空,已知反应①-⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120。
(1)写出A、B的化学式
A__________________ B____________________
(2)写出下列化学反应方程式或离子方程式:
反应③的化学方程式_________________________________________________
反应⑤的离子方程式_________________________________________________
(3)写出反应①所使用设备的名称_________________________________
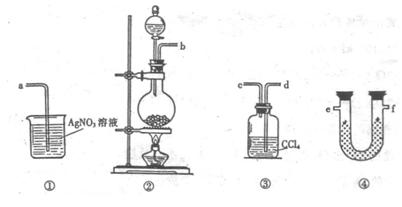
 b接 , 接
, 接a。
b接 , 接
, 接a。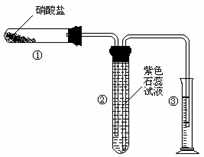
 (Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,
(Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,