摘要:20.通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱.也可用于估算化学反应的反应热(△H).化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差. 化学键 Si-O Si-Cl H-H H-Cl Si-Si Si-C 键能/ KJ·mol-1 460 360 436 431 176 347 请回答下列问题: (1)比较下列两组物质的熔点高低Y(填>或<=SiC Si, SiCl4 SiO2 (2)右图立方体中心的“● 表示硅晶体中的一个原子. 请在立方体的顶点用“● 表示出与之紧邻的硅原子. (3)工业上高纯硅可通过下列反应制取: SiCl4 (g) + 2H2 该反应的反应热△H = KJ/mol 21.根据反应框图填空.已知反应①-⑤均为工业生产及应用中常见反应.其中B.G.I.J.L均为常见单质.B.D.J.L为气体.A是工业生产F的重要矿石原料的主要成份.其相对分子质量为120. (1)写出A.B的化学式 A B (2)写出下列化学反应方程式或离子方程式: 反应③的化学方程式 反应⑤的离子方程式 (3)写出反应①所使用设备的名称
网址:http://m.1010jiajiao.com/timu3_id_38571[举报]
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的焓变(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
|
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的反应热等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
请回答下列问题:
(1)已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列两组物质的熔点高低(填“>”或“<”):SiC
(2)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)
Si(s)+4HCl(g),
则2mol H2生成高纯硅需
查看习题详情和答案>>
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/ kJ?mol-1 |
460 | 360 | 436 | 431 | 176 | 347 |
(1)已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列两组物质的熔点高低(填“>”或“<”):SiC
>
>
Si,Si<
<
SiO2(2)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)
| ||
则2mol H2生成高纯硅需
吸收
吸收
(填“吸收”或“放出”)能量236
236
kJ. 通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H).
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H).| 化学键 | Cl-Cl | H-H | H-Cl | N≡N |
| 键能/kJ?mol | 243 | 436 | 431 | 946 |
a 2HCl(g)=H2(g)+Cl2(g);△H=
+183kJ/mol
+183kJ/mol
b N2(g)+3H2(g)=2NH3(g)△H=-92kJ/mol,则N-H键的键能是
391
391
kJ?mol(2)1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
NO2(g)+CO(g)=CO2(g)+NO(g)
NO2(g)+CO(g)=CO2(g)+NO(g)
△H=-234kJ?mol-1
△H=-234kJ?mol-1
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1
②2CO (g)+O2(g)=2CO2(g)△H2
③H2O(g)=H2O(l)△H3
则CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
(4)已知:2Al (s)+
| 3 |
| 2 |
2Fe (s)+
| 3 |
| 2 |
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式
2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H=-828.42kJmol-1
2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H=-828.42kJmol-1
. 通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
(1)比较下列两组物质的熔点高低(填“>”或“<”)SiC
(2)如图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子.
(3)工业上用高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
| ||
21.通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/ kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
⑴ 比较下列两组物质的熔点高低(填>或<)
SiC______ Si; SiCl4 ______ SiO2
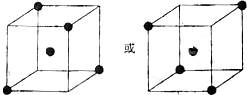
⑵ 图立方体中心的“●”表示硅晶体中的一个原子,
请在立方体的顶点用“●”表示出与之紧邻的硅原子。
⑶ 工业上高纯硅可通过下列反应制取:
SiCl4 (g) + 2H2(g) ![]() Si(s) + 4HCl(g)
Si(s) + 4HCl(g)
该反应的反应热△H = ___________ KJ/mol