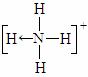23.(10分)下表是元素周期表的前三周期,用相应的化学用语回答下列问题:
|
|
|
|
|
|
|
|
|
|
a |
|
|
b |
c |
d |
e |
|
|
f |
|
g |
|
|
|
|
|
(1)g的单质能与f元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式 。
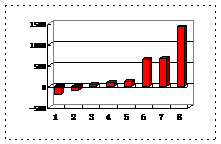
(2)第三周期8种元素按单质熔点(℃)大小顺序的柱形图(上左图),其中序列“2”代表 ,“8”代表 。
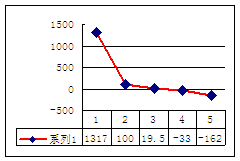
(3)a、b、c、d、e的氢化物的沸点直角坐标图(上右图),序列“5”氢化物的化学式为 ,序列“1”的氢化物的电子式: 。
22.(8分)现有A、B、C、D、E五种原子序数依次增大的短周期元素。已知:A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的邻族元素;D和E的原子序数之和为30;它们两两形成的化合物有甲、乙、丙、丁四种,这四种化合物中原子个数比如下表:
|
|
甲 |
乙 |
丙 |
丁 |
|
化合物中各元素原子个数比 |
A∶C = 1∶1 |
B∶A = 1∶2 |
D∶E = 1∶3 |
B∶E = 1∶4 |
回答下列问题:
(1)甲分子的电子式为 ;丁分子的空间构型为 。
(2)已知:乙分子中所有原子共平面,则实验室制取乙的化学方程式为
。
(3)丙的水溶液加热蒸干再灼烧,最后所得固体的成分是 (写化学式)
21.(10分)《2004年江苏省环境公报》指出:2004年全省废水排放总量为46.6亿吨,其中工业废水排放量为26.3亿吨,生活污水排放量为20.3亿吨。废水中化学需氧量(COD)排放总量为85.4万吨,其中工业废水中COD排放量为29.8万吨,占COD排放总量的34.9%;生活污水中COD排放量为55.6万吨,占COD排放总量的65.1%。氨氮排放总量为7.3万吨,石油类排放总量为1804.3吨,挥发酚排放总量为74.3吨。
回答下列问题:
(1)江苏省水污染的特征是___________________________________________________________。
(2)某校研究性学习小组拟选择“本地水污染情况分析”的课题进行探究。
①如果你参加该课题的探究,写出你的子课题名称和你选择该子课题的理由:___________________________________________________________________________ ______________________________________。
②水中的NO2-是含氮有机物分解的产物,其浓度的大小是水源污染的标志之一。检测水中的NO2-可用比色法,其步骤是:
(Ⅰ)配制标准溶液:称取0.30gNaNO2,溶于水后在容量瓶中稀释至1L得溶液A,移取5mL溶液A,稀释至1L,得溶液B。
(Ⅱ)配制标准色阶:取6只规格为10mL的比色管(即质地、大小、厚薄相同且具塞的平底试管),分别加入体积不等的溶液B,并稀释至10mL,再加入少许(约0.3g)氨基苯磺酸(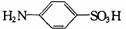 )粉末,实验结果如下表所示。
)粉末,实验结果如下表所示。
|
色阶序号 |
1 |
2 |
3 |
4 |
5 |
6 |
|
加入溶液B的体积(mL) |
0.0 |
2.0 |
4.0 |
6.0 |
8.0 |
10.0 |
|
反应后溶液颜色 |
由无色变为由浅到深的樱桃红色 |
(Ⅲ)检测:取10mL水样倒入比色管中,加少许氨基苯磺酸,显色后与标准色阶对比。
请填写以下空白:
a.比色法的基本依据是 ;
b.若水样显色后与色阶中的5号颜色相同,则表明水样中含NO2-含量为 mg/L。
c.用NaNO2直接配制溶液B的缺点是 。
d.如果水样显色后比6号还深,应采取的措施是 。
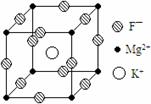 (10分)某种晶体的晶胞为立方体,结构如右图所示:
(10分)某种晶体的晶胞为立方体,结构如右图所示: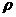 g/cm3,阿伏加德罗常数用NA表示,求算晶体中两个距离最近的Mg2+中心间距离。
g/cm3,阿伏加德罗常数用NA表示,求算晶体中两个距离最近的Mg2+中心间距离。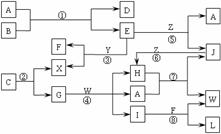 Ⅲ.B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且质量分数都是28%,组成B的金属元素原子核外的K层和M层电子数相同。
Ⅲ.B和C都是由一种金属与一种非金属元素组成的化合物,其中非金属元素相同且质量分数都是28%,组成B的金属元素原子核外的K层和M层电子数相同。