0 37100 37108 37114 37118 37124 37126 37130 37136 37138 37144 37150 37154 37156 37160 37166 37168 37174 37178 37180 37184 37186 37190 37192 37194 37195 37196 37198 37199 37200 37202 37204 37208 37210 37214 37216 37220 37226 37228 37234 37238 37240 37244 37250 37256 37258 37264 37268 37270 37276 37280 37286 37294 447348
 C(g)。若开始时通入1molA和1mol B,达到平衡后生成a mol C,则下列说法错误的是
C(g)。若开始时通入1molA和1mol B,达到平衡后生成a mol C,则下列说法错误的是 2NH3达到平衡的标志是
2NH3达到平衡的标志是 (A)32.把下列物质分别加入盛水的锥形瓶内,立即塞紧带U形管的塞子。已知U形管内预先装有少量水且液面相平(为便于观察,预先染成红色),加入下列哪些物质后,发生如图所示变化①NaOH粉末;②18mol/L的H2SO4溶液;③NH4NO3晶体;④Na2O2固体;⑤生石灰
(A)32.把下列物质分别加入盛水的锥形瓶内,立即塞紧带U形管的塞子。已知U形管内预先装有少量水且液面相平(为便于观察,预先染成红色),加入下列哪些物质后,发生如图所示变化①NaOH粉末;②18mol/L的H2SO4溶液;③NH4NO3晶体;④Na2O2固体;⑤生石灰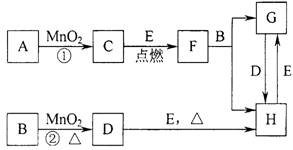 ⑴写出有关物质的名称或化学式:
⑴写出有关物质的名称或化学式: pC(g)中,m、n、p为系数,且m+n>p,正反应是放热反应。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是
pC(g)中,m、n、p为系数,且m+n>p,正反应是放热反应。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是
 ( D )9.对于达平衡的可逆反应X+Y
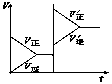
( D )9.对于达平衡的可逆反应X+Y W+Z,增大压强则正、逆反应速率(v)的变化如图,分析可知X、Y、Z、W的聚集状态可能是
W+Z,增大压强则正、逆反应速率(v)的变化如图,分析可知X、Y、Z、W的聚集状态可能是 氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题:
氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置部分均略去)。回答下列问题: