网址:http://m.1010jiajiao.com/timu3_id_371973[举报]
(15分)砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩.
(1)基态砷原子的电子排布式为_______________,砷与溴的第一电离能较大的是______.
(2)AsH3是无色稍有大蒜味气体.AsH3的沸点高于PH3,其主要原因是
________________________________________________.
(3)Na3AsO4可作杀虫剂.AsO43-的空间构型为_____________,与其互为
等电子体的一种分子为______________.
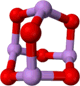
(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示,该化合物的分子式为__________,As原子采取_______杂化.

(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与_______个Ga相连,As与Ga之间存在的化学键有_____________(填字母)。
A.离子键 B.氢键 C.配位键 D.金属键 E.极性键
查看习题详情和答案>>
已知33As、35Br位于同一周期。某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是 。已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式是 。
(2)在该反应条件下可推知 (填序号)。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X d.还原性:X>AsH3
(3)该反应的氧化剂和还原剂的物质的量之比为__________; KBrO3与HBr反应也会生成X,则该反应中氧化剂和还原剂的物质的量之比为__________。
查看习题详情和答案>>
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩.
(1)基态砷原子的电子排布式为________;砷与溴的第一电离能较大的是________.
(2)AsH3是无色稍有大蒜味气体.A sH3的沸点高于PH3,其主要原因是________.
(3)Na3AsO4可作杀虫剂.AsO43-的空间构型为________,与其互为等电子体的一种分子为________.
(4)某砷的氧化物俗称“砒霜”,其分子结构如图所示.该化合物的分子式为________,As原子采取________杂化.
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似.GaAs晶体中,每个As与________个Ga相连,As与Ga之间存在的化学键有________(填字母).
A.离子键
B.σ键
C.π键
D.氢键
E.配位键
F.金属键
G.极性键
| 元素 | 相关信息 |
| X | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
| Y | 地壳中含量最高的元素 |
| Z | 存在质量数为23,中子数为11的核素 |
| W | 生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质 |
| R | 有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X与氢两元素按原子数目比1:3和2:4构成分子A和B,A的结构式为




(3)砷(As)是人体必需的微量元素,与X同一主族,As原子比X原子多两个电子层,则砷的原子序数为
(4)用RCl3溶液腐蚀铜线路板的离子方程式为
(5)Z-W合金(Z17W12)是一种潜在的贮氢材料,由Z、W单质在一定条件下熔炼而成.该合金在一定条件下完全吸氢的反应方程式为:Z17W12+17H2═17ZH2+12W,得到的混合物Q(17ZH2+12W)在6.0mol/L HCl溶液中能完全释放出H2.1mol Zl7W12完全吸氢后得到的混合物Q与上述盐酸完全反应,释放出H2的物质的量为
(1)砷化镓是一种半导体材料,其化学式为
(2)写出As原子处于基态时的核外电子排布式
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与
(4)NH3是氮的氢化物,中心原子的杂化方式是