4.氯的含氧酸及其钠盐的性质
|
化合价 |
酸分子式 |
酸的强度 |
热稳定性 |
氧化性 |
盐的化学式 |
热稳定性 |
氧化性 |
|
+1 +3 +5 +7 |
HClO HClO2 HClO3 HClO4 |
| 增 | 强 |  ↓ ↓ |
| 增 | 强 |  ↓ ↓ |
| 减 | 弱 |  ↓ ↓ |
NaClO NaClO2 NaClO3 NaClO4 |
| 增 | 强 |  ↓ ↓ |
| 减 | 弱 |  ↓ ↓ |
|
热稳定性 |
酸<盐 |
||||||
|
氧化性 |
酸>盐 |
3.卤化物的性质和制法
|
项 目 |
化学性质 |
|
制备方法 |
|
跟金属反应 (氧化性) |
Fe+CuCl2 Cu+FeCl2 Cu+FeCl22FeCl3+Cu  2Fe
Cl2+CuCl2 2Fe
Cl2+CuCl2 |
金属与卤 素反应 |
2Al+3Cl2 2AlCl3 2AlCl32Fe+3Cl2  2FeCl3 2FeCl3 |
|
跟非金属反应(置换反应) |
2NaBr+Cl2 2NaCl+Br2 2NaCl+Br22KI+Br2  2KBr+I2 2KBr+I2 |
金属与氢卤酸反应 |
2Al+6HCl 2AlCl3+3H2↑
2AlCl3+3H2↑Fe+2HCl  FeCl2+H2↑ FeCl2+H2↑ |
|
跟碱反应 (复分解反应) |
MgCl2+2NaOH 2NaCl+ 2NaCl+Mg(OH)2↓ CuBr2 +2NaOH  Cu(OH)2↓ Cu(OH)2↓+2NaBr |
金属氧化物与氢卤酸反应 |
Fe2O3+6HCl 2FeCl3+3H2O 2FeCl3+3H2OCuO+2HCl  CuCl2+H2O CuCl2+H2O |
|
跟酸反应(复分解反应) |
CaF2+H2SO4(浓)  CaSO4+2HF↑ 2NaCl+H2SO4(浓)  Na2SO4+2HCl↑ Na2SO4+2HCl↑ |
盐与氢卤酸反应 |
CaCO3+2HCl CaCl2+H2O+CO2↑ CaCl2+H2O+CO2↑AgNO3+HCl  AgCl↓+HNO3 AgCl↓+HNO3 |
|
跟盐反应(复分解反应) |
NaCl+AgNO3 AgCl↓+NaNO3 AgCl↓+NaNO3CaCl2+2NaF  CaF2↓+2NaCl CaF2↓+2NaCl |
盐与卤素反应 |
MgSO4+BaCl2 MgCl2+BaSO4↓ MgCl2+BaSO4↓AgNO3+KBr  AgBr↓+KNO3 AgBr↓+KNO3 |
|
分解反应 |
2AgBr 2Ag+Br2 2Ag+Br22AgI  2Ag+I2 2Ag+I2 |
碱与氢卤酸反应 |
NaOH+HCl NaCl+H2O NaCl+H2OMg(OH)2+2HBr  MgBr2+2H2O MgBr2+2H2O |
2.卤化氢的结构、性质、制法和用途
|
元素名称和符号 |
HF(氟化氢、氢氟酸) |
HCl(氯化氢、氢氯酸) |
HBr(溴化氢、氢溴 酸) |
HI(碘化氢、氢碘酸) |
|||
|
结构 |
结构与晶体 |
直线型分子、分子晶体 |
直线型分子、分子晶体 |
直线型分子、分子晶体 |
直线型分子、分子晶体 |
||
|
键的极性 |
-------极性递减-----→ |
||||||
|
分子的极性 |
-------极性递减-----→ |
||||||
|
键能 |
-------递 减-----→ |
||||||
|
物理性质 |
稳定性 |
最稳定 |
稳定 |
不太稳定 |
不太稳定 |
||
|
熔点、沸点 |
-83.0℃, 19.5℃ |
-114.6℃, -84.1℃ |
-88.5℃ -67℃ |
-50.9℃ -35.0℃ |
|||
|
水溶液酸性 |
弱酸 |
强酸 |
强酸 |
强酸 |
|||
|
化学性质 |
与金属反应 |
盐+H2 |
盐+H2 |
盐+H2 |
盐+H2 |
||
|
与碱性氧化物反应 |
盐+H2O |
盐+H2O |
盐+H2O |
盐+H2O |
|||
|
与碱反应 |
盐+H2O |
盐+H2O |
盐+H2O |
盐+H2O |
|||
|
与AgNO3反应 |
不反应 |
Ag++Cl- AgCl↓(白色) AgCl↓(白色) |
Ag++Br- AgBr↓(淡黄) AgBr↓(淡黄) |
Ag++I- AgI↓(黄色) AgI↓(黄色) |
|||
|
与Ca2+反应 |
Ca2++2HF CaF2↓+2H+ |
不反应 |
不反应 |
不反应 |
|||
|
X-的还原性 |
很弱 |
很弱 |
较强 |
较强 |
|||
|
制法 |
CaF2+H2SO4(浓)  CaSO4+2HF↑H2+ F2 CaSO4+2HF↑H2+ F2 2HF 2HF |
2NaCl+H2SO4(浓)  Na2SO4+2HCl↑H2+Cl2 Na2SO4+2HCl↑H2+Cl2 2HCl 2HCl |
NaBr+H3PO4(浓)  NaH2PO4+HBr↑ NaH2PO4+HBr↑H2+Br2  2HBr 2HBr |
NaI+H3PO4(浓)  NaH2PO4+HI↑H2+I2 NaH2PO4+HI↑H2+I2 HI(难) HI(难) |
|||
|
用途 |
制氢氟酸、工艺业 |
制盐酸、H2、氯化物 |
制氢溴酸、溴化物 |
制氢 碘酸、碘化物 |
|||
|
特性 |
银盐 |
溶于水 |
不溶于水 |
不溶于水 |
不溶于水 |
||
|
钙盐 |
不溶于水 |
溶于水 |
溶于水 |
溶于水 |
|||
|
检验 |
Ca2++2F- CaF2↓(白) CaF2↓(白) |
Ag++Cl- AgCl↓(白)
AgCl↓(白) |
Ag++Br- AgBr↓(淡黄)
AgBr↓(淡黄) |
Ag++I- AgI↓(黄) AgI↓(黄) |
|||
1.卤族元素原子结构、单质性质、制法和用途:
|
元素名称和符号 |
氟(F) |
氯(Cl) |
溴(Br) |
碘(I) |
||||||||||
|
原子 结构 |
原子序数 |
9 |
17 |
35 |
53 |
|||||||||
|
结构示意图 |
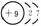 |
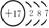 |
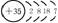 |
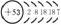 |
||||||||||
|
电子式 |
·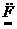 ∶ ∶ |
·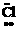 ∶ ∶ |
·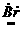 ∶ ∶ |
·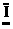 ∶ ∶ |
||||||||||
|
主要化合价 |
-1 |
-1,+1,+3,+5,+7 |
-1,+1,+3,+5 |
-1,+1,+3,+5 |
||||||||||
|
相同点 |
最外层电子数相同,都是7个电子 |
|||||||||||||
|
不同点 |
原子核外电子层数不同,依次增大 |
|||||||||||||
|
原子半径 |
--------递增--------→ |
|||||||||||||
|
阴离子半径 |
--------递增--------→ |
|||||||||||||
|
非金属活动性 |
--------递减--------→ |
|||||||||||||
|
原子氧化能力 |
--------递减--------→ |
|||||||||||||
|
阴离子还原能力 |
--------递增--------→ |
|||||||||||||
|
物 理性 质 |
颜色和状态 |
浅黄绿色气体 |
黄绿色气体 |
红棕色液体易挥发 |
紫黑色固体易升华 |
|||||||||
|
密度 |
1.69克/升 |
3.214克/升 |
3.119克/厘米3 |
4. 93克/厘米3 |
||||||||||
|
熔点(℃) |
--------递增--------→ |
|||||||||||||
|
沸点(℃) |
--------递增--------→ |
|||||||||||||
|
水中溶解性 |
分解水 |
--------递减--------→ |
||||||||||||
|
有机溶剂 |
分解溶剂 |
-------溶解性增大-----→ |
||||||||||||
|
化学反应` |
与金属反应 |
nX2+2M 2MXn 与大多数金属反应 反应快慢F2>Cl2>Br2>I2 2MXn 与大多数金属反应 反应快慢F2>Cl2>Br2>I2 |
||||||||||||
|
与H2反应 |
X2+H2 2HX 反应剧烈程度 F2>Cl2>Br2>I2 2HX 反应剧烈程度 F2>Cl2>Br2>I2 |
|||||||||||||
|
与磷反应 |
2P+3X2 2PX3(X2不足量) 2P+5X2 2PX3(X2不足量) 2P+5X2 2PX5(X2足量) 2PX5(X2足量) 现象:白色烟雾 |
|||||||||||||
|
与H2O反应 |
2H2O+2F2 4HF+O2 4HF+O2(使水迅速分解) |
Cl2+H2O HCl+HClO (反应较慢) |
Br2+2H2O HBr HBr+HBrO (反应很慢) |
I2+H2O HI+HIO (反应不明显) |
||||||||||
|
与NaOH反应 |
2F2+4NaOH 4NaF+O2+ 4NaF+O2+2H2O |
X2+2NaOH NaX+NaXO+H2O NaX+NaXO+H2O(X=Cl,Br,I) |
||||||||||||
|
置换反应 |
分解水 |
X2+2Y- 2X-+Y2 (Y=Br,I)置换能力(Cl2>Br2>I2) 2X-+Y2 (Y=Br,I)置换能力(Cl2>Br2>I2) |
||||||||||||
|
制法 |
2KHF2 F2↑+H2↑+2KF F2↑+H2↑+2KF |
2NaCl+2H2O 2NaOH+H2↑+Cl2↑(工业) 2NaOH+H2↑+Cl2↑(工业)MnO2+4HCl(浓)  Cl2↑+MnCl2+2H2O(实验室) Cl2↑+MnCl2+2H2O(实验室) |
2NaBr+Cl2  2NaCl+Br2 2NaCl+Br22NaBr+MnO2+3H2SO4  Br2↑+2NaHSO4+MnSO4+2H2O Br2↑+2NaHSO4+MnSO4+2H2O |
2KI+Cl2 2KCl+I2 2KCl+I22NaI+H2SO4+MnO2  MnSO4+2NaHSO4+I2+2H2O |
||||||||||
|
特性与检验: |
F2:能跟氙、氡等惰性气体反应生成XeF2,KrF2,通入水中产生O2 |
Cl2:本身呈黄绿色,氯水常用于杀菌消毒,与AgNO3反应生成AgCl白色沉淀 |
Br2:与皮肤接触产生疼痛而难治愈,与AgNO3反应生成淡黄色AgBr沉淀 |
I2:使淀粉溶液变蓝,与AgNO3溶液反应生成黄色AgI沉淀 |
||||||||||
|
用途: |
提炼铀 |
制盐酸、塑料农药、漂白粉 |
染料工业、制AgBr制溴化物 |
碘酒、AgI、碘仿 制碘化物 |
||||||||||