0 35413 35421 35427 35431 35437 35439 35443 35449 35451 35457 35463 35467 35469 35473 35479 35481 35487 35491 35493 35497 35499 35503 35505 35507 35508 35509 35511 35512 35513 35515 35517 35521 35523 35527 35529 35533 35539 35541 35547 35551 35553 35557 35563 35569 35571 35577 35581 35583 35589 35593 35599 35607 447348
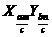
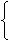 达到两个规定
规定配制溶液里所含溶质的量
达到两个规定
规定配制溶液里所含溶质的量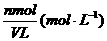
 )
)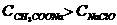 ,因为等物质的量浓度CH3COONa和NaClO溶液,NaClO水解程度大)
,因为等物质的量浓度CH3COONa和NaClO溶液,NaClO水解程度大)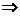 引伸:
引伸: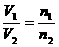
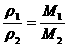
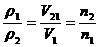

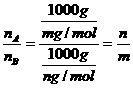 ,C中同温同压密度比等于其式量比,应为m:n,因此正确答案为A、B、C。
,C中同温同压密度比等于其式量比,应为m:n,因此正确答案为A、B、C。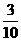 ,
,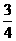 (2x+y-4)
(2x+y-4) 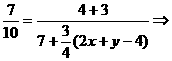 2x+y=8,即x=2, y=4合理,因此化学式为N2H4。
2x+y=8,即x=2, y=4合理,因此化学式为N2H4。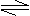 (5)不对,因为2NO2 N2O4+Q,标况下(温度低)NO2部分转化为N2O4,气体
(5)不对,因为2NO2 N2O4+Q,标况下(温度低)NO2部分转化为N2O4,气体