|
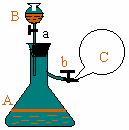
1. (8分)如图所示,在支管锥形瓶A中充满等体积的H2S和NO气体;在分液漏斗B中盛有淀粉碘化钾溶液;在锥形瓶的支管处用弹簧夹b夹紧,并充满O2的气球C。根据实验,填写:
|
(1).打开分液漏斗的活塞a,将漏斗中的溶液缓慢的流入A中,
发生的变化是:( H2S 气体溶于KI溶液中 )。
请判断:( )
(2).松开弹簧夹b,气球C逐渐_________,
锥形瓶A中的气体 颜色立即变成__________. ( )
(A)增大 棕色 (B)缩小 红色
(C)缩小 棕色 (D)增大 红色
(3).锥形瓶A中的溶液开始变混浊,这是因为______.
(用化学方程式表示)。 ( )
(A)2NO + O2 = 2NO2 (B) H2S + 2NO2 = 2HNO3 + S
(C)2KI + 2NO2 = 2KNO3 + I2 (D)以上都不对。
(4).锥形瓶A中的溶液开始变混浊,在溶液中变混浊的同时,
溶液出现浅蓝色,这是因为( )
(A)2NO + O2 = 2NO2 (B)H2S + 2NO2 = 2HNO3 + S
(C)2KI + 2NO2 = 2KNO3 + I2 (D)以上都不对。
2. (共15分)在实验室中制取少量乙酸乙酯的主要步骤如下:
① 把2毫升乙醇、1毫升浓硫酸装入反应的试管中,再加入2毫升10% 的醋酸。
② 在收集试管中,装入饱和的NaOH 溶液,组装好全部装置。
③ 将反应试管加强热,保持剧烈沸腾。
④ 倒出收集试管中的上层液体,即得到产品乙酸乙酯。
指出以上①-④步骤中的主要错误,并回答有关问题:
错误处:
① ________________________________________________________________________,
②________________________________________________________________________,
③________________________________________________________________________,
④________________________________________________________________________,
问题:
(1).步骤③操作的作用是(应小心加热,使酯化反应充分进行,并把乙酸乙酯蒸出)。
判断对错:( )
(2).收集试管中的导管为什么不能插入溶液中?
[答]:
(3).乙酸乙酯的主要用途是_________________,___________________。
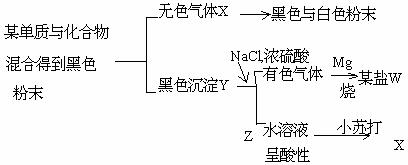 3.(6分) 根据下列图示,回答问题。
3.(6分) 根据下列图示,回答问题。
(1).原两种黑色粉末的名称是(碳)和(二氧化锰);
判断对错:( )
W 盐的化学式为( ALCL3 )。
判断对错:( )
(2). X 与Mg 的反应的化学方程式为: CO2 + 2Mg = 2MgO + C.
判断对错:( )
(3). Z 溶液呈酸性的主要原因是NaHSO4 = Na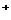 + H
+ H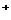 + SO
+ SO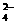 .
.
判断对错: ( )
 和 bY
和 bY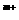 两种简单离子(X、Y全都是短周期元素),已知X
两种简单离子(X、Y全都是短周期元素),已知X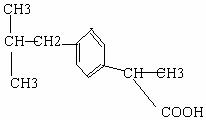 7. 具有解热镇痛及抗生素作用的药物“芬必得”,
7. 具有解热镇痛及抗生素作用的药物“芬必得”,
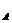 为阿伏加德罗常数,下列叙述正确的是( )
为阿伏加德罗常数,下列叙述正确的是( )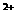 失去的电子数目为0.1N
失去的电子数目为0.1N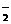 离子中含有的电子数为 0.8N
离子中含有的电子数为 0.8N