24、(9分)在一个固定体积的密闭容器中,保持一定温度,进行以下反应:
H2(g)+Br2(g)≒2HBr(g)
已知加入1molH2和2molBr2时,达到平衡后生成amolHBr(见下表“已知”项)。在相同条件下,且保持平衡时各组分的摩尔分数不变,对下列编号(1)~(3)的状态,填写表中的空白:
|
编号 |
起始状态(mol) |
平衡时HBr物质的量 (mol) |
||
|
H2 |
Br2 |
HBr |
||
|
已知 |
1 |
2 |
0 |
a |
|
⑴ |
2 |
4 |
0 |
|
|
⑵ |
|
|
1 |
0.5a |
|
⑶ |
m |
N(n≥2m) |
|
|
23、(8分)已知,向Zn2+离子溶液中滴加氨水,生成Zn(OH)2白色沉淀;但是氨水过量时,沉淀又溶解,生成了Zn(NH3)42+。此外,Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液中,生成ZnO22-,所以Zn(OH)2是一种两性氢氧化物。
现有4组离子,每组有2种金属离子。请各选用1种试剂,将它们两者分开。可供选用的试剂有:A 硫酸 B 盐酸 C 硝酸 D 氢氧化钠溶液 E 氨水(填写时用字母代号)
请填写下表:
|
离子组 |
选用的试剂(代号) |
沉淀物的化学式 |
保留在溶液中的离子 |
|
⑴Zn2+和Al3+ |
|
|
|
|
⑵Zn2+和Mg2+ |
|
|
|
|
⑶Zn2+和Ba2+ |
|
|
|
|
⑷Fe3+和Al3+ |
|
|
|
 ФCHO
NaOH,乙醇溶液
ФCHO
NaOH,乙醇溶液 CH3CHO
CH3CHO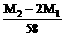 B、n=
B、n=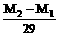 C、n=
C、n=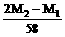 D、n=
D、n=