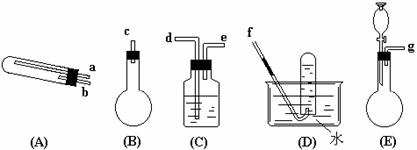
6. 实验室可用NH4HCO3和NaCl为原料制备纯碱。请根据下表数据和实验步骤,回答下列问题:
30℃时几种盐的溶解度(克/100克水)
|
NaCl |
NH4HCO3 |
NH4Cl |
NaHCO3 |
Na2SO4 |
(NH4)2SO4 |
CaCl2 |
MgCl2 |
CaSO4 |
|
36.3 |
27.0 |
41.4 |
11.1 |
40.8 |
78.0 |
51.7 |
26.2 |
0.165 |
制备纯碱的主要步骤如下:
①配制50毫升约25%的粗食盐水(密度近似为1克/厘米3);
②精制食盐水(粗食盐中含有少量Ca2+、Mg2+、SO42-等杂质),用盐酸将滤液的pH值调节至7;
③加热食盐水,将溶液温度控制在30-35℃;
④在不断搅拌下,分数次将研细的NH4HCO3加入食盐水中,加完料后,继续保温、搅拌半小时;
⑤静置,趁热过滤,回收母液,晶体用蒸馏水洗涤两次;
⑥将晶体灼烧,得到纯碱。
(1) 步骤①中,配制溶液的最后一步操作是 [说明:用不着容量瓶、用不着定容,因为该过程不需要非常精确:“配制50毫升约25%的粗食盐水”]
(2) 步骤②中,SO42-是否需要除去? ,理由是 ;
(3) 步骤④中所有操作的共同目的是 ;
(4) 步骤⑤中晶体的洗涤液中主要含有的杂质阳离子是 [注意:是“杂质阳离子”;Ca2+、Mg2+在精制的过程中已经除去,而Na+不是杂质离子],在通常情况下,检验这种阳离子的方法是 。
 7. 某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质。整个实验过程如下,请回答有关问题:
7. 某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质。整个实验过程如下,请回答有关问题:
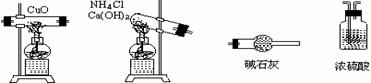
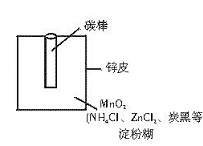
(1) 干电池的基本构造和工作原理。
上图为干电池的基本构造图。干电池工作时负极上的电极反应式是 。
正极上的电极反应式是___________(已知NH4+的得电子能力大于Zn2+)。
MnO2作去极剂(吸收正极放出的H2,防止产生极化现象),该反应方程式为:H2+2MnO2=Mn2O3+H2O。而淀粉糊的作用是提高阴、阳离子在两个电极的迁移速率。
正极产生的NH3又和ZnCl2溶液作用:Zn2++4NH3=[Zn(NH3)4]2+
(2) 锌皮和碳棒的回收。用钳子和剪刀剪开回收的干电池的锌铜,将锌皮和碳棒取出,并用毛刷刷干净,将电池内的黑色粉末移入小烧杯中。
(3) 氯化铵、氯化锌的提取、检验和分离。
①如何从黑色粉末中提取NH4Cl和ZnCl2等晶体的混合物?写出简要的实验步骤:
②设计简单的实验证明所得晶体中含有NH4+。
实验步骤:
实验现象:
有关的离子方程式: 。
③用什么方法可将NH4Cl和ZnCl2的晶体混合物分离开? 。
(4) 最后剩余的黑色残渣的主要成分是MnO2,还有炭黑和有机物等。可用灼烧的方法除去杂质,该实验中需要用到的主要仪器有 。
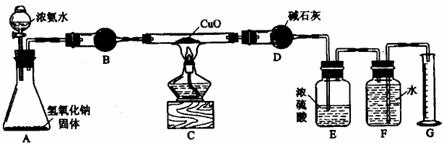
 2NH3 (4)碱石灰;除去HCl和水蒸气 (5)防止水倒吸进入D中加热的试管中,兼收集NH3的作用 (6)酚酞溶液;溶液由无色变成红色
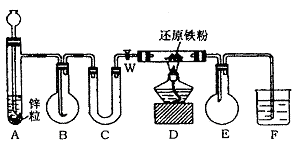
2NH3 (4)碱石灰;除去HCl和水蒸气 (5)防止水倒吸进入D中加热的试管中,兼收集NH3的作用 (6)酚酞溶液;溶液由无色变成红色 N2+3Cu+3H2O (2)NaOH的强碱性及溶解产生的热利于氨气的逸出。 (3)C (4)黑色粉末变为光亮的红色固体。 (5)将反应剩余的氨吸收。 (6)3a/22.4 9a/11.2b (7)减小,D装置吸收的水中包含了从A中带出的水份。
N2+3Cu+3H2O (2)NaOH的强碱性及溶解产生的热利于氨气的逸出。 (3)C (4)黑色粉末变为光亮的红色固体。 (5)将反应剩余的氨吸收。 (6)3a/22.4 9a/11.2b (7)减小,D装置吸收的水中包含了从A中带出的水份。