②将另一部分红色固体加足量的4摩/升硫酸溶液,轻轻振荡,经足够长的时间以后,溶液呈蓝色,还有相当多的紫红色固体未溶解。
根据上述实验现象回答或填空:
(1) 解释在实验①中产生红棕色气体及溶液变蓝的现象(用简要的文字和化学方程式说明该现象)
(2) 解释实验②中紫红色固体不溶的现象。
(3) 解释实验②中溶液变蓝的原因。
(4) 由上述分析可以得知氧化铜被氢气还原可能分两步进行,写出这两步反应的化学方程式。
3. 有1、2.3、4号四瓶未知溶液,它们是:NaCl(0.1mol/L)、HCl(0.1mol/L)、NaOH(0.1mol/L)、酚酞(0.1%),有人不用其它试剂,就把它们-一鉴别开来了。其实验步骤如下:
(1) 各取少许溶液两两混和,据此分成两组;
(2) 取一组混和液,不断滴入另一组中的一种未知液,据此可鉴别出1号和2号;
(3) 再取已鉴别出的1号2mL,滴入3滴3号未知液,再加4号未知液4mL,在这个过程中无明显实验现象。
综合以上实验,可以确认1号是 ,2号是 ,3号是 ,4号是 。
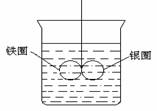 4. 如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处,吊着一根绝缘的细丝,使之平衡。小心地从烧杯中央滴入CuSO4溶液。
4. 如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处,吊着一根绝缘的细丝,使之平衡。小心地从烧杯中央滴入CuSO4溶液。
(1) 片刻后观察到的现象是(指金属圈)__________.
A. 铁圈和银圈左右摇摆不定
B. 保持平衡状态不变
C. 铁圈向下倾斜
D. 银圈向下倾斜
(2) 产生上述现象的原因是
.
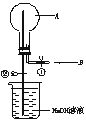 5. 如图所示,在一个烧瓶中充满气体A,打开①处的止水夹并向烧瓶中缓慢通入等体积的气体B后关闭该止水夹,待充分反应后再打开②处的止水夹。请按要求填表回答打开②处的止水夹前后烧瓶中观察的现象并按要求书写反应的化学方程式:
5. 如图所示,在一个烧瓶中充满气体A,打开①处的止水夹并向烧瓶中缓慢通入等体积的气体B后关闭该止水夹,待充分反应后再打开②处的止水夹。请按要求填表回答打开②处的止水夹前后烧瓶中观察的现象并按要求书写反应的化学方程式:
(1) 填写下列表格:
|
实验
序号 |
气体A |
气体B |
现 象 |
A与B反应 的化学方程式 |
|
|
打开②处止水夹前 |
打开②处止水夹后 |
||||
|
① |
SO2 |
H2S |
---- |
|
|
|
② |
NH3 |
HCl |
|
|
|
|
③ |
O2 |
NO |
|
|
|
 (2) 分别完成以上三个实验后,烧瓶内剩余气体最多的是(填实验序号) 。
(2) 分别完成以上三个实验后,烧瓶内剩余气体最多的是(填实验序号) 。
1] (1)NaHCO3是从含大量NH4+、Na+、Cl-、HCO3-离子的饱和溶液中析出的,所以NaHCO3晶体中混有杂质,由于NaCl受热时不发生变化,导致工业纯碱中常含有少量的NaCl。
|
分析与计分 |
计算样品中碳酸钠的质量分数 |
对实验结果的评价 |
实验失败的主要原
因及对结果的影响 |
|
甲组 |
84.8% |
失败 |
所生成的CO2没有被全部吸收,有一部分滞留在反应容器中,导致测定结果偏低。 |
|
乙组 |
95.4% |
成功 |
/ |
|
丙组 |
95.4% |
成功 |
/ |
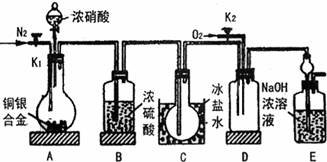
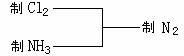 8. 某探究性学习小组在查阅资料中发现,常温下氯气可以氧化氨气获得氮气。该小组由此设计出制取氮气的思路:
8. 某探究性学习小组在查阅资料中发现,常温下氯气可以氧化氨气获得氮气。该小组由此设计出制取氮气的思路:
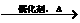 4NO+6H2O (3)0.5mol/L NaOH溶液和酚酞试液(或⑧、⑨) 红色褪去 (4)安全(或防止液态物质冲出) (5)6mol/LNaOH溶液(或⑦) 吸收氮的氧化物
4NO+6H2O (3)0.5mol/L NaOH溶液和酚酞试液(或⑧、⑨) 红色褪去 (4)安全(或防止液态物质冲出) (5)6mol/LNaOH溶液(或⑦) 吸收氮的氧化物