21.(12分)下表由元素周期表的前三周期去掉副族上方的空白区域后组合而成,表中虚线处为ⅡA、ⅢA族的连接处,请用相应的化学用语或符号回答下列问题:
|
a |
|
|
|
|
|
|
|
|
b |
|
|
c |
d |
e |
f |
|
|
g |
|
h |
|
|
|
|
|
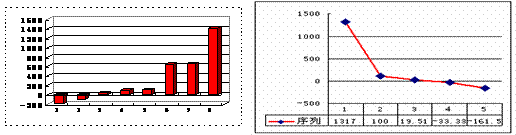
图(1) 图(2)
(1)上图(1)是表示第三周期8种元素单质的熔点(℃)柱形图,已知柱形“1”代表Ar,则其中柱形“8”代表的是 晶体(填晶体的类型)。
(2)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(2),序列“5”的氢化物的名称是
序列“2”的氢化物的结构式为 。
(3)e元素与f元素相比,电负性f大于e,下列表述中能证明这一事实的是 (填选项序号)
A.常温下f单质的颜色比e单质的颜色深
B.f单质与e的氢化物剧烈反应,产生e的单质
C.f与e形成的化合物中e元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目‘
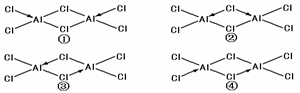 (4)科学家证实,氯化铝属于共价化合物,分子式为Al2Cl6,其结构式为下列四种中的一种,你认为正确的结构是_______________。
(4)科学家证实,氯化铝属于共价化合物,分子式为Al2Cl6,其结构式为下列四种中的一种,你认为正确的结构是_______________。
 (5)叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定方面越来越引起人们的重视,由叠氮化钠(Sodium azida)NaN3热分解可得光谱纯N2:2NaN3(s)→2Na(l)+3N2(g),有关说法正确的是_____________(选填序号)
(5)叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定方面越来越引起人们的重视,由叠氮化钠(Sodium azida)NaN3热分解可得光谱纯N2:2NaN3(s)→2Na(l)+3N2(g),有关说法正确的是_____________(选填序号)
A.NaN3与KN3结构类似,前者晶格能较小
B.钠晶胞结构如右图,晶胞中分摊2个钠原子
C.氮的电负性大于氧 D.Na+的半径小于N3-的半径
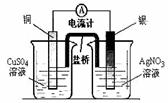
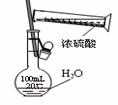
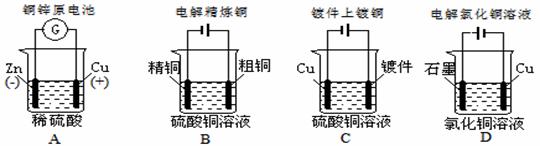 下列图示中关于铜电极的连接错误的是
下列图示中关于铜电极的连接错误的是 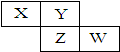 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示。若Z原子的最外层电子数是K层电子数的3倍,下列说法中正确的是
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示。若Z原子的最外层电子数是K层电子数的3倍,下列说法中正确的是 Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。它与我们的生活密切相关。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。它与我们的生活密切相关。 “华安、连城、永安、漳平,龙海二中,泉港一中”六校联考
“华安、连城、永安、漳平,龙海二中,泉港一中”六校联考